Болезнь Крона: что это такое, симптомы, лечение, диагностика, причины, признаки
Определение.
Что такое болезнь Крона
Болезнь Крона - заболевание с трансмуральным характером поражения, с преимущественным поражением дистальной части подвздошной и толстой кишки, при котором однако может быть поражен любой отдел ЖКГ. Это хроническая неспецифическая сегментарная воспалительная и гранулематозно-язвенная патология кишечника.
Симптоматика включает диарею и боль в животе. Могут развиваться абсцессы, внутренние и внешние фистулы, кишечная непроходимость. Есть вероятность внекишечных проявлений, в особенности артриты. Диагноз устанавливают с помощью колоноскопии и контрастных исследований с барием. Лечение проводится препаратами 5-АСК, кортикостероидами, иммуномодуляторами, антицитокиновыми препаратами, антибиотиками; нередко требуется хирургическое вмешательство.
Патофизиология болезни Крона
В целом БК можно назвать аутоиммунным заболеванием. Это значит, что ваша иммунная система, которая в норме борется с инфекциями, нападает на ваш кишечник, вызывая появление язв и воспаления кишки, что приводит к проявлению болезни. Причина БК — в сочетании нескольких факторов, которые мы только начинаем понимать. Наиболее вероятно, что болезнь становится следствием ряда причин, включая генетику, воздействие окружающей среды, дефектов иммунной системы и взаимодействие с кишечными бактериями. Однозначно можно утверждать, что ваше ВЗК вызвал не один фактор, а, напротив, сочетание нескольких причин.
Для понимания патофизиологии этих заболеваний необходимо представление о развитии патологического процесса, поскольку причиной БК могут быть множество факторов или их сочетание. К ним относятся:
- генетические факторы;
- иммунная система;
- кишечный микробиом;
- окружающая среда.
Генетические факторы
Первым открытым в 2001 г. геном, связанным с ВЗК, стал ген NOD2, расположенный в локусе IBD1. С этого времени тщательный полногеномный анализ выявил более 160 генов, ассоциированных с ВЗК, и их число постоянно растет. Участие генетики в ВЗК позволяют предположить также распространенность заболевания в пределах семьи и расовые и этнические различия. Наиболее часто ВЗК развивается у европеоидов. Подтверждена также и, этническая предрасположенность: заболевание наиболее распространено среди еврейского населения, особенно среди ашкеназских евреев. Все эти закономерности указывают на участие генетических факторов в развитии ВЗК.
Иммунная система
Иммунная система включает три основных компонента, которые действуют вместе для защиты организма от микробов и инородных частиц, называемых антигенами. Иммунная система состоит из:
- выстилки желудочно-кишечного тракта — слизистой оболочки (эпителия). Помимо своей функции как физического барьера, эпителий также выделяет слизь и другие антибактериальные вещества. Это в сочетании с перистальтикой кишечника способствует удалению вредных микроорганизмов;
- врожденной иммунной системы, представленной преимущественно белыми клетками крови (нейтрофилами, эозинофилами, базофилами и макрофагами) и естественными киллерами. Эти клетки несут рецепторы, которые связываются со специфическими рецепторами микробов или продуктами их жизнедеятельности и нейтрализуют их;
- адаптивной иммунной системы (клеточная память), представленной В-лимфоцитами, Т-лимфоцитами и дендритными клетками. В-лимфоциты выделяют антитела, а Т-лимфоциты, взаимодействуя с антигенами, запускают иммунный ответ, опосредованный цитокинами. Дендритные клетки содействуют Т- и В-лимфоцитам в распознавании вредных антигенов.
Предполагается, что нарушение функции иммунной системы влияет на развитие ВЗК следующим образом.
- Нарушение целостности кишечного эпителия, проницаемости, секреции слизи, количества бактерий и аномальная переработка антигенов иммунной системой, все или по отдельности, могут играть роль в развитии ВЗК. Повышенная проницаемость кишечника приводит к притоку нейтрофилов, макрофагов и лимфоцитов, что вызывает усиленный воспалительный ответ. Исследования также свидетельствуют о повышении экспрессии молекул адгезии на иммунных клетках и об их связывании с эпителием.
- При ВЗК выявляется повышенное число В-лимфоцитов, а следовательно, и увеличенное количество антител, направленных против нормальных антигенов организма (ауто-антител). К примеру, в ходе множества исследований было установлено, что при ЯК чаще, чем при БК, обнаруживаются перинуклеарные антитела к цитоплазме нейтрофилов и отсутствуют антитела к Saccharomyces cerevisiae (чувствительность 57%, специфичность 97%). Схожим образом наличие антител к Saccharomyces cerevisiae и отсутствие антител к цитоплазме нейтрофилов более характерны для пациентов с БК, чем для больных ЯК (чувствительность 49%, специфич ность 97%).
- Т-лимфоциты преимущественно представлены CD4+ (Т-хелперами) и CD8+ (цитотоксическими) клетками. Т-хелперы в зависимости от функции подразделяются на Th1-, Тh2- и Th1-клетки. Thl-клетки преимущественно оказывают провоспалительное действие, выделяя активные вещества, например интерферон-γ и фактор некроза опухоли (ФНО)-α. Th17-клетки играют важную роль в воспалении и аутоиммунитете. Th2-клетки способствуют регуляции ответа В-лимфоцитов на антигены.
- Клетки иммунной системы выделяют медиаторы воспаления — цитокины. Цитокины играют ключевую роль в воспалении: они стимулируют клетки к выработке большего количества подобных веществ, способствуют миграции лимфоцитов и ан гиген-презентирующих клеток к очагу воспаления, тем самым вызывая характерные патологические изменения в тканях. Как при ЯК, так и при БК регуляция этого воспалительного ответа нарушена, что и приводит к хроническому воспалению.
Кишечный микробиом
Кишечник человека насыщен микробной флорой (микробиотой), особенно в дистальных отделах тонкой кишки — подвздошной кишке и в толстой кишке. Эта флора состоит из нормальных кишечных бактерий, способствующих здоровью нашего организма, и вредных патогенных бактерий. Соотношение этой флоры поддерживается целостностью эпителия и иммунной системы. Любое нарушение этого равновесия может привести к воспалению. Такие изменения происходят под действием патогенных бактерий или продуктов их жизнедеятельности, при нарушении целостности или исходном повреждении эпителия, а также при аномальном иммунном ответе на продукты жизнедеятельности микробов.
Пусковые факторы внешней среды
Чрезмерное употребление мясной пищи и ненасыщенных жиров, недостаточный прием витамина D, прием антибиотиков и другие факторы могут способствовать развитию и/или обострению ВЗК. Впрочем, это установлено неокончательно и нуждается в дополнительных исследованиях.
Причины болезни Крона
Этиология этого заболевания неизвестна, однако предполагают, что его могут провоцировать следующие факторы: инфекции (туберкулезная, вирусная), аллергии и аутоаллергии, наследственная предрасположенность, аутоиммунные механизмы — формирование аутоантител к клеткам слизистой оболочки кишечника. В развитии заболевания не исключается и предрасполагающая роль кишечного дисбиоза. Болезнь Крона дебютирует в молодом и зрелом возрасте (20—60 лет) и значительно снижает качество жизни и социальную активность таких пациентов.
Симптомы и признаки болезни Крона
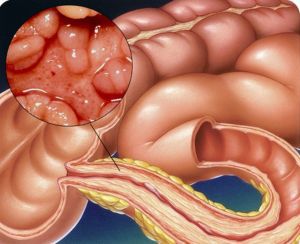
Болезнь Крона может поражать любой отдел кишечника — от ротовой полости до анального канала, но преимущественно вовлекает в патологический процесс подвздошную и ободочную кишку. Воспаление обычно начинается вокруг кишечных желез, называемых криптами, что вначале приводит к образованию поверхностных язв. Позднее эти язвы увеличиваются в продольном и поперечном направлении по поверхности слизистой оболочки, а также проникают глубже в стенку кишки, придавая кишке вид «булыжной мостовой». Воспаленные участки кишки чередуются со здоровыми участками, формируя характерное прерывистое поражение. Воспаление может затрагивать всю толщу кишечной стенки (распространяться трансмуралъно). Патогномоничной для БК является неказеозная гранулема, представляющая собой скопление лимфоцитов и макрофагов в кишечной стенке. Эти изменения на микроскопическом уровне неизбежно приводят к следующим симптомам и осложнениям.
- Боль в животе: присутствует вне зависимости от распространения болезни. Она возникает вследствие трансмурального характера заболевания или в связи с осложнениями, например кишечной непроходимостью.
- Диарея: частое проявление БК. Воспаление может повышать кишечную секрецию, приводя к нарушенному всасыванию и диарее. Укорочение кишки у пациентов, перенесших операцию, часто приводит к диарее.
- Кровотечение: нередко в стуле обнаруживается кровь. Для БК также характерно скрытое кровотечение.
- Свищи: образуются вследствие трансмурального характера заболевания. Они представляют собой патологические ходы между кишкой и мочевым пузырем, кишкой и кожей, разными кишками или между кишкой и влагалищем. Свищи могут протекать бессимптомно или проявляться инфекциями мочевыводящих путей при сообщении кишки с мочевым пузырем, выделением кала из влагалища или на брюшную стенку при сообщении с кожей. Частота образования свищей достигает 33-50%.
- Кишечная непроходимость: трансмуральное поражение приводит к фиброзу кишечной стенки, что вызывает сужение ее просвета — образованию стриктуры, что, в свою очередь, приводит к кишечной непроходимости.
- Перианальные проявления: возникновение кожных складок-рубцов*, свищи, анальные трещины и абсцессы перианальной области. До 1/3 больных БК страдают перианальной формой заболевания, которая часто плохо поддается лечению.
- Нарушения всасывания: чаще всего возникает в результате воспаления терминального отдела подвздошной кишки или после ее хирургической резекции, вызывающей потерю желчных кислот со стулом и связанную с этим «билиарную диарею». Вследствие потери желчных кислот ослабляется всасывание жира, что приводит к стеаторее — появлению жирного стула. Мальабсорбция также может способствовать образованию камней в желчном пузыре и почках.
Клинически выделяют определенные формы этого заболевания.
Аппендикулярную, которая характеризуется болями, поносами, кровотечениями, гиповитаминозом, электролитными нарушениями. Боль не локализована, ее характер зависит от причины, обусловливающей ее возникновение. Так, при изъязвлении гранулем она носит схваткообразный характер; при перфорации кишки и развитии перитонита боль острая, возникает при перемене положения тела, прикосновении к животу, она крайне интенсивна, сопровождается рефлекторной рвотой. В период обострения заболевания диарея отмечается до 10 раз в сутки: стул жидкий, обильный, содержит примесь слизи, а при формировании язв — и крови. При локализации патологического процесса в толстой кишке могут возникать болезненные позывы на низ (тенезмы). Нередко к указанным симптомам присоединяются и другие признаки заболевания (артралгии, лихорадка).
Лихорадочную, при которой температура тела повышается порой до фебрильных величин и сопровождается появлением общих признаков заболевания — утомляемости, головной боли, вялости, снижения аппетита.
В клинической картине артралгической формы заболевания преобладают боли и припухлость в коленных, локтевых, тазобедренных суставах; при этом кишечные проявления заболевания могут отсутствовать или быть выраженными незначительно, способны присоединяться к артралгическим проявлениям заболевания несколько позже.
При отечной форме в клинической картине заболевания преобладают отеки.
Выявляют глубокие язвы, часто возникающие как прямые трещины. Глубокие язвы могут пенетрировать кишечную стенку и инициировать развитие абсцесса, свища.
Характерна неоднородность изменений. Даже когда повреждён относительно короткий сегмент кишечника, воспалительный процесс прерывается островками нормальной слизистой оболочки с внезапным переходом от изменённой части к интактной. Таким образом, небольшой участок поражения отделяется от повреждённой области — так называемое перескакивающее поражение. Брыжеечные лимфатические узлы увеличены, а брыжейка утолщена.
Имеются фокальные скопления эпителиоидных гистиоцитов, окружённые лимфоцитами и содержащие гигантские клетки. Выявляют также лимфоидные скопления или микрогранулёмы. Если они располагаются близко к поверхности слизистой оболочки, то они часто изъязвляются и формируют небольшие афтозоподобные язвы.
Поражение аногенитальной области может проявиться за несколько лет до желудочно-кишечных симптомов заболевания и представлять серьезные диагностические трудности.
Отек часто бывает первым симптомом поражения вульвы, к другим его проявлениям относятся развитие абсцессов, язв, свищей. Свищевой ход может сообщаться с заднепроходным каналом и прямой кишкой, вызывая недержание кала; его наружное отверстие имеет вид язвы с утолщенными гладкими краями.
Диагностика болезни Крона
- Рентгеновские исследования с барием желудка, тонкой и толстой кишок.
- КТ брюшной полости (обычная или в режиме КТ-энтерографии).
- В ряде случаев - магнитно-резонансная (MP) энтерография, эндоскопия и/или колоноскопия.
В крови отмечаются лейкоцитоз, увеличение СОЭ, гипо-и диспротеинемия, гипохромная железодефицитная анемия различной степени выраженности. При осмотре боль при пальпации локализуется преимущественно в правой подвздошной области, там же часто прощупывается опухолевидное болезненное образование.
БК следует заподозрить при наличии признаков воспаления или непроходимости, а также при отсутствии выраженной симптоматики со стороны ЖКТ, но при наличии перианальных фистул или абсцессов либо артрита неясного происхождения, узловатой эритемы, лихорадки, анемии, задержки роста (у детей). Семейный анамнез болезни Крона повышает вероятность ее наличия. Сходные проявления могут наблюдаться при других заболеваниях ЖКТ. Дифференциальная диагностика с ЯК может представлять сложности в 20% случаев, когда БК протекает с поражением толстой кишки. Однако из-за сходных принципов лечения дифференциальная диагностика принципиальна в основном только в случаях, когда решается вопрос хирургического вмешательства или экспериментального лечения.
При развитии «острого живота» (при первой атаке или при обострении) необходимо проводить рентгенографию брюшной полости в положении лежа и стоя, а также КТ брюшной полости. В ходе данных исследований можно выявить признаки непроходимости, абсцессы, фистулы и другие возможные причины «острого живота» (в частности, аппендицит). УЗИ помогает проводить дифференциальную диагностику с гинекологическими заболеваниями у женщин.
При наличии менее острых первоначальных проявлений более предпочтительно, чем КТ, проведение рентгенографии верхних отделов ЖКТ с оценкой пассажа бария по тонкой кишке и прицельными снимками терминального отдела подвздошной кишки. Однако в некоторых центрах диагностическими методами выбора становятся более новые технологии КТ- или МР-энтерографии, при которых удается получить изображения высокого разрешения в условиях приема большого объема контрастного вещества. Данные методы фактически являются диагностическими, если с их помощью выявлены характерные стриктуры или фистулы с «отключенными петлями» кишечника. При наличии спорных изменений проводится КТ-энтерография или видеокапсульная энтероскопия, при которой могут определяться авты или линейные язвы. При преобладании признаков поражения толстой кишки (в частности, диареи) может определяться рефлюкс бария в терминальный отдел подвздошной кишки с неравномерностью сужения просвета, бугристыми контурами, утолщением и ригидностью стенки. При подобных изменениях нужно проводить дифференциальный диагноз с раком слепой кишки, карциноидом подвздошной кишки, лимфомой, системным васкулитом, лучевым энтеритом, туберкулезом илеоцекальной зоны, амебомой.
При атипичных проявлениях(преобладании диареи, минимальной выраженности боли) план обследования аналогичен таковому при подозрении на ЯК с проведением колоноскопии (с биопсией, забором образцов на исследование кишечных патогенов). При эндоскопии верхних отделов ЖКТ могут определяться признаки мягковыраженного поражения даже в отсутствие симптоматики, характерной для поражения верхних отделов.
Лабораторные исследования проводят с целью выявления анемии, гипоальбуминемии, электролитного дисбаланса. Оценивают функциональные печеночные тесты; повышение щелочной фосфатазы и γ-глутамилтранспептидазы при распространенном поражении толстой кишки позволяет заподозрить первичный склерозирующий холангит. Лейкоцитоз и повышение острофазовых показателей (СОЭ, С-ре-активного белка) не являются специфическими признаками, но могут применяться для контроля активности болезни.
Перинуклеарные антинейрофильные антитела обнаруживают в 60-70% случаев при ЯК и лишь в 5-20% при БК. Антитела к Saccharomyces cerevisiae относительно специфичны для болезни Крона. Все же определение антител не позволяет надежно различить ЯК и БК. При недифференцированном колите их диагностическая ценность остается неопределенной, поэтому данные тесты не рекомендованы для применения в ежедневной практике.
Дифференциальная диагностика болезни Крона
Из общих проявлений заболевания преобладают симптомы похожие на симптомы язвенного колита, поэтому их дифференциальная диагностика представляет большие трудности. Однако при ректороманоскопии и морфологическом исследовании обнаруживаются специфические изменения. В частности, для начальных проявлений заболевания характерна инфильтративная фаза: отек и инфильтрация кишечной стенки с сужением просвета кишки, исчезновением поперечной складчатости, появлением мелких эрозий с наложением фибрина. Разгар болезни соответствует фазе трещин. Это уже деструктивный процесс с образованием язв и псевдополипов. Фазе клинической ремиссии соответствует стадия рубцевания, при которой слизистая приобретает рельеф булыжной мостовой: втяжения сочетаются с нормальной слизистой. При болезни Крона поражается вначале не слизистая оболочка, а подслизистый слой с образованием гранулем. Описаны случаи поражения двенадцатиперстной кишки и желудка.
Прогноз болезни Крона
БК практически не поддается полному излечению и характеризуется чередованием обострений и ремиссий. Возможно тяжелое течение с частыми изнуряющими периодами боли. Однако при обоснованном подборе лекарственных средств и, при наличии показаний, хирургическом лечении удается поддерживать удовлетворительное качество жизни и адаптивные возможности у большинства пациентов. Смертность при болезни Крона характеризуется как очень низкая. Дополнительные причины летальных исходов, связанных с БК, связаны с развитием злокачественных опухолей ЖКТ, в т.ч. рака толстой и тонкой кишок.
Лечение болезни Крона
Болезнь Крона — воспалительное заболевание, при котором иммунная система атакует кишечник, приводя к воспалению и изъявлению. Это вызывает боль в животе, диарею, лихорадку, слабость и другие симптомы. У некоторых пациентов с БК появляются свищи (гнойные ходы, соединяющие кишечник с окружающей кожей или другими органами). Считается, что повреждение тканей при БК вызывают преимущественно белые клетки крови, поэтому большинство видов лечения направлены на то, чтобы или напрямую остановить их производство, или замедлить их привлечение и проникновение в кишечник. Генетические исследования позволяют предположить, что такое «нападение» на кишку является попыткой иммунной системы воздействовать на бактерии и другие организмы, находящиеся в кишке.
При выборе «наилучшего из возможных» способа лечения БК ваш врач должен учесть следующие факторы: где в организме активизировалась БК, какова тяжесть воспаления и помогали (или нет) ранее назначавшиеся лекарственные препараты, а также курите ли вы (и как много), отягощена ли ваша наследственность и выполнялись ли вам операции. К сожалению, долгие годы единственным эффективным способом лечения оставались стероиды (т.е. преднизолон и гидрокортизон), которые помогают лишь на время уменьшить воспаление. Однако стероиды неэффективны в долгосрочной перспективе, а также обладают существенными побочными эффектами, что заставляет нас применять другие препараты. Будесонид — стероид с меньшей частотой побочных эффектов; его стараются назначать вместо преднизолона или гидрокортизона, но и он непригоден для долгосрочного применения.
В настоящее время пациентам с БК доступны четыре основные группы препаратов; во многих случаях ваш врач может использовать несколько лекарств для достижения наилучшего результата. К этим четырем группам лекарственных средств относятся следующие.
- Антибиотики. Наиболее часто используются ципрофлоксацин и метронидазол. Они являются важным компонентом лечения активных инфекций, свищей и абсцессов («гнойных затеков»), но также могут помочь пациентам с частичным нарушением проходимости кишечника, уменьшая боль, газообразование, вздутие и диарею, возникающие из-за размножения бактерий выше уровня суженного просвета кишки.
- Противовоспалительные препараты. К ним относятся такие препараты, как сульфасалазин и похожие на него таблетки, клизмы и свечи с месалазином. К сожалению, они эффективны лишь при очень легкой форме БК.
- Иммуносупрессоры. Азатиоприн и очень похожий на него меркаптопурин — эффективные таблетированные лекарственные средства, действующие на выработку белых клеток крови. Из-за того, что их эффект развивается не сразу, их часто назначают одновременно с быстродействующими препаратами (такими как стероиды), а затем применяют длительно для поддержания ремиссии заболевания. Другим вариантом лечения является метотрексат, обычно назначаемый в виде небольших подкожных инъекций 1 раз в неделю (или в виде таблеток). Иммуносупрессоры обычно назначают пациентам, получающим биологическую терапию (см. далее), чтобы предотвратить образование антител к биологическим препаратам.
- Биологические препараты. Все они в настоящее время доступны или для внутривенного введения, или для подкожных инъекций. Наиболее часто применяется группа средств, блокирующих ФНО, преимущественно и вызывающий повреждение кишечника. Из этих быстродействующих препаратов при БК используют адалимумаб, цертолизумаба пэгол и инфликсимаб. Новым классом являются блокаторы «молекул адгезии», которые эффективно препятствуют выходу белых клеток крови из кровотока и их проникновению в кишечник, а также блокируют некоторые другие их функции. К таким биологическим препаратам относятся натализумаб и ведолизумаб; их действие развивается несколько медленнее, однако из-за их локального воздействия только на пораженные органы на них возлагают большие надежды.
Важно понимать, что БК является хроническим рецидивирующим заболеванием, которое возобновится при прекращении эффективного лечения. Как следствие, лечение, которое однажды помогло, обычно стараются долгое время не прекращать. Единственным исключением являются стероиды, которые применяются только кратковременно.
Принимая во внимание прогрессирующий характер БК, ее медикаментозная терапия направлена на регуляцию нарушенного воспалительного ответа и имеет цель изменить естественное течение болезни. Долгое время единственные доступные препараты — кортикостероиды и сульфасалазин — оказались неспособны изменить естественное течение заболевания. От них выгодно отличаются иммуносупрессоры и биологические препараты, которые продемонстрировали способность препятствовать прогрессированию множества вариантов БК, поворачивая течение болезни вспять. Имея возможность изменить естественное течение этого прогрессирующего желудочно-кишечного заболевания, мы можем назначать терапию с целью вызвать (индуцировать) и поддержать эндоскопическую (и гистологическую) ремиссию.
При выборе наиболее подходящей терапии для впервые выявленной БК мы сталкиваемся с рядом вопросов: назначение аминосалицилатов, попытка отказа от кортикостероидов, раннее применение биологических препаратов и комбинация биологических средств и иммуносупрессоров.
Аминосалицилаты
Сульфасалазин и лекарственные формы месалазина показали различные результаты в исследованиях их эффективности при лечении активной БК. Метаанализ плацебо-контролируемых испытаний этих препаратов, применявшихся более 16 нед при активной БК, выявил статистически значимое, но клинически незначимое уменьшение активности заболевания, оцениваемое индексом активности БК. Возможность их применения в качестве поддерживающей терапии не подтвердилась. В целом роль месалазина ограничивается применением только при легкой БК, а их эффективность следует подтвердить при периодической оценке активности заболевания эндоскопически и/или рентгенологически).
Кортикостероиды
Кортикостероиды заслуженно пользуются дурной славой при лечении БК; хотя они способны на время устранить некоторые симптомы, они не влияют на течение заболевания, а их долгосрочные побочные эффекты могут быть катастрофическими. Будесонид, доступный в форме капсул с контролируемым растворением в подвздошной кишке, воздействует на тонкую кишку и правые отделы ободочной кишки. Этот препарат оказался сопоставим по эффективности индукции клинической ремиссии с преднизолоном (53% против 66%), при пом побочные эффекты развивались существенно реже. Эффективность будесонида в поддержании ремиссии пока не доказана; систематический обзор по применению будесонида в качестве противорецидивной терапии не подтвердил его эффективность через 3 мес после достижения ремиссии.
Тиопурины
Тиопурины (азатиоприн и меркаптопурин) относятся к препаратам с медленным развитием эффекта. Индукция ремиссии обычно требует применения быстродействующих кортикостероидов или биологических препаратов. Доказано, что лечение тиопуринами позволяет отказаться или сократить применение стероидов, хотя этот эффект и проявляется спустя 3 мес после начала приема. Исследования, продемонстрировавшие развитие клинического обострения после отмены тиопуринов, подтверждают их эффективность для долгосрочного контроля заболевания. В то же время монотерапия тиопуринами, согласно исследованиям, не влияет на исход лечения впервые выявленной БК и связана с развитием редких лимфопролиферативных заболеваний, миелодегенеративных заболеваний и немеланоматозного рака кожи.
Метотрексат
Метотрексат также требует одновременного назначения быстродействующих препаратов для индукции ремиссии БК (таких, как кортикостероиды или биологические препараты). Исследование 16-недельного применения инъекционного метотрексата (25 мг 1 раз в неделю) в сравнении с плацебо продемонстрировало, что частота клинической ремиссии (определялась как <150 баллов по индексу активности БК) была выше в группе метотрексата, чем в группе плацебо (39,4% против 19,1). При изучении поддерживающей терапии у больных, достигших клинической ремиссии, она чаще сохранялась у пациентов, рандомизированных в группу метотрексата (65%), чем у получавших плацебо (39%). Таким образом, применение метотрексата было эффективным средством индукции и поддержания ремиссии в эпоху до начала использования биологических препаратов.
Ингибиторы фактора некроза опухоли
Появление биологических препаратов радикальным образом изменило тактику лечения и методы оценки эффективности препаратов в клинических испытаниях. Эти препараты подтвердили свою эффективность и в индукции, и в поддержании терапии. Кроме того, биологическая терапия позволила ввести концепцию раннего агрессивного медикаментозного лечения пациентов с коротким анамнезом заболевания и факторами, прогнозирующими развитие осложнений. Метаанализ 10 исследований показал, что в сравнении с плацебо анти-ФНО-терапия приводит к увеличению вероятности индукции ремиссии (относительный риск: 1,66; 95% доверительный интервал: 1,17-2,36) и ее поддержания (относительный риск: 1,78, 95% доверительный интервал: 1,51-2,09). Кроме того, недавно проведенные исследования указывают на вероятность 4-летней бесстероидной ремиссии и снижения частоты госпитализаций и операций при регулярных введениях анти-ФНО-препаратов. Нежелательные реакции не включают развитие злокачественных новообразований, а риск тяжелых инфекций составляет 0,64 на 100 пациенто-лет (сопоставим с традиционными средствами лечения БК). Это позволяет рекомендовать биологическую терапию в качестве первоначального средства лечения пациентов с плохим прогнозом.
Антиинтегрины
Антитела к интегринам также имеют доказанную эффективность при индукции и поддержании ремиссии у пациентов с БК. Первоначальный энтузиазм в применении натализумаба, использовавшегося при рассеянном склерозе (так как препарат связывает молекулы адгезии в центральной нервной системе), быстро прошел с появлением сообщений о развитии инвалидизирующих и смертельных случаев прогрессирующей мультифокальной лейкоэнцефалопатии. Последовавшие исследования установили, что это заболевание является осложнением инфекции вирусом Джона Каннингема (JC-вирус). Современная тактика применения этих лекарств требует исследования крови на антитела к вирусу. Если они отсутствуют, возможно назначение монотерапии натализумабом, однако ее следует прекратить, если в дальнейшем анализ крови пациента становится «положительным» на JC-вирус (анализ повторяют каждый год или полгода). Долгосрочная эффективность натализумаба при БК, в том числе не ответивших на инфликсимаб, оставляют этот препарат в арсенале резервных средств терапии.
На смену натализумабу в середине 2014 г. пришел ведолизумаб. Этот антиинтегрин воздействует только на кишку: случаи прогрессирующей мультифокальной лейкоэнцефалопатии на фоне такой терапии не описаны и не ожидаются. Его применение, несмотря на превосходный профиль безопасности, ограничивается непродолжительным применением на рынке, а также несколько замедленным развитием действия по сравнению с анти-ФНО-препаратами.
Комбинированная терапия
Принимая во внимание частоту успешного применения биологической терапии, современное лечение БК ставит целью усилить и продлить ответ на данные препараты. После подтверждения образования антител к биологическим лекарственным средствам, уменьшающегося при сопутствующем приеме иммуносупрессоров, появились рекомендации по ранней комбинированной иммуносупрессии. В ходе открытого 2-летнего исследования 133 пациента были рандомизированы для получения сочетанной терапии азатиоприном и инфликсимабом (с периодическими введениями последнего) или лечения по стандартной схеме с применением кортикостероидов, а затем азатиоприна и инфликсимаба. Частота бесстероидной ремиссии через 26 нед составила 60% в группе комбинированной иммуносупрессии по сравнению с 35,9% в группе «традиционной» терапии. В проведенном затем исследовании SONIC 508 больных среднетяжелой и тяжелой БК рандомизировали, они получали монотерапию инфликсимабом, азатиоприном или комбинированную иммуносупрессию. Конечная точка исследования — бесстероидная ремиссия на 26-й неделе — была достигнута у 56,8% получавших комбинированное лечение, у 44,4% получавших инфликсимаб и у 30% принимавших только азатиоприн. Кроме того, заживление слизистой оболочки отмечалось у 43,9% в группе комбинированной терапии, у 30,1% — в группе монотерапии инфликсимабом и у 16,5% — среди принимавших азатиоприн.
Все более широкое применение и признание роли биологической терапии привело к накоплению опыта ее оптимального применения и мониторинга лекарственной терапии. Наилучший ответ на терапию достигается при раннем назначении биологических препаратов, проведении регулярной, а не эпизодической, поддерживающей терапии, сопутствующем применении иммуносупрессоров, а также при использовании премедикации для подавления выработки антител к биологическим лекарственным средствам. Кроме того, широко внедряемый мониторинг уровня препарата привел к получению результатов, указывающих на возможность прогнозировать клинический ответ на основании этого уровня. В будущем методика оптимизации алгоритма терапии и применение новых лекарственных средств с объективным мониторингом активности заболевания будет изучаться все шире.
Целенаправленная терапия для поддержания стойкой клинико-эндоскопической ремиссии ставит задачей прервать прогрессирующее деструктивное течение болезни, которое завершается развитием недостаточности пищеварения и иных осложнений заболевания. Выбор исходной терапии должен включать индивидуальный ее подбор, чтобы назначать наиболее мощные препараты пациентам в группе высокого риска. Хотя операция и не приводит к исцелению пациента, к ней придется прибегать в сложных случаях, и при четком определении к ней показаний она может привести к продолжительному контролю над заболеванием. В будущих исследованиях будет продолжено изучение оптимизации лекарственной терапии для создания персонализированного алгоритма на основании активности заболевания и мониторинга терапии, а целью лечения станет изменение естественного течения заболевания.
Этиопатогенетическое лечение не проводится. Симптоматическая терапия осуществляется в зависимости от тяжести заболевания. Наиболее часто используется сульфасалазин — препарат с выраженным противовоспалительным и антимикробным действием на стенку кишечника. Лекарство может оказывать угнетающее воздействие на систему кроветворения, поэтому во время терапии необходимо периодически проводить общий анализ крови. Доза препарата рассчитывается индивидуально с учетом тяжести заболевания. Во время ее обострения суточная доза может достигать 4 г. Поддерживающая суточная доза составляет 0,5 г — ее делят на 3 приема, принимают после употребления пищи. Диета при болезни Крона соблюдается постоянно, особенно строго — при обострении патологического процесса. Исключаются грубая клетчатка, продукты, вызывающие диарею (персики, инжир, курага, слива, продукты, богатые жирами — особенно животного происхождения). Строго ограничиваются прием алкоголя и курение. Симптоматически применяют антидиарейные препараты — лоперамид, смектит диоктаэдрический, адсорбенты — активированный уголь, полифепан. Тяжелое течение заболевания обусловливает необходимость использования глюкокортикоидов из расчета 0,5—1 г/кг массы тела в сутки. Указанная доза применяется для купирования обострения (1—2 месяца), а затем постепенно снижается и сводится к поддерживающей — до 10 г в сутки (1 месяц). Хроническая гипохромная железодефицитная анемия лечится согласно общим принципам с использованием препаратов железа.
Иногда для ускорения заживления необходимо ограниченное иссечение измененных тканей. При неспецифическом язвенном колите кожа аногенитальной области поражается значительно реже, хотя иногда наблюдается пустулезная вегетирующая сыпь в паху.
Активная фаза
Эффективны и аминосалицилаты, и глюкокортикоиды, обычно вызывающие ремиссию при активном илеоколите и колите. При тяжёлых формах показан преднизолон внутривенно, но перед назначением глюкокортикоидов необходимо исключить абсцесс или образование свища. Диетотерапия с использованием полимерных или базисных диет при болезни Крона вызывает ремиссию. Возможные механизмы включают устранение пищевых антигенов, других, определяющих болезнь, иммунологических дефектов и неспецифические эффекты питательной поддержки. Длительная диетотерапия с исключением нормального питания затруднительна для пациентов; частота ремиссий сопоставима с достигнутыми результатами терапии глюкокортикоидами, но частота рецидивов выше, и, за исключением педиатрической практики, первичную диетотерапию сегодня используют редко.
Будесонид подходит для лечения умеренно активного процесса, хотя он менее эффективен в низких дозах. Аминосадицилаты не приносят дополнительной пользы, но есть некоторые основания продолжать использование перорального метронидазола.
Инфликсимаб противопоказан при инфекции, включая туберкулёз, и может давать осложнения в виде аллергических реакций. Рецидив обычно возникает через 12 нед после лечения, и по этой причине инфликсимаб комбинируют с препаратами, модифицирующими болезнь: или тиопуринами, или метотрексатом — для поддержания ремиссии. Инфликсимаб (в отличие от глюкокортикоидов) вызывает значительное восстановление слизистой оболочки, но это может приводить к образованию рубцов и стриктур. Поэтому он с осторожностью используется у пациентов со стенозирующими процессами.
Лечение пациентов с диффузным и распространённым заболеванием подвздошно-толстокишечной локализации представляет значительные терапевтические сложности. Комбинация медикаментозной терапии, питательной поддержки, включающей длительное парентеральное питание, хирургического вмешательства и эндоскопической баллонной дилатации стриктур может понадобиться в любое время.
Образование свищей и патология перианальной области
Свищ обычно образуется вследствие активной болезни Крона и связан с сепсисом. Первый шаг в лечении — определить участок свищеобразования, для этого может потребоваться рентгенография с барием, КТ и МРТ. Необходимо хирургическое вмешательство, хотя во многих случаях достаточно лечения лежащего в основе активного заболевания глюкокортикоидами и питательной поддержки. При простом перианальном поражении терапия первой линии — метронидазол и/или ципрофлоксацин. Тиопурины используют при хроническом заболевании.
Показано, что инфликсимаб, вводимый с интервалом 4—8 нед, излечивает кишечно-кожные свищи.
Поддержание ремиссии
Более эффективная, чем любые фармакологические вмешательства, мера — отказ от курения.
У аминосалицилатов отмечают минимальную эффективность. Пациентов с рецидивами более 1 раза в год лечат тиопуринами. Пациентам у которых непереносимость и резистентность к азатиоприну назначают метотрексат 1 раз в нед в комбинации с фолиевой кислотой. Пациентов с агрессивным течением заболевания лечат комбинацией иммуномодулирующих препаратов и инфликсимаба.
Следует избегать хронического использования глюкокортикоидов, так как это приводит к остеопении и другим побочным эффектам, не предотвращая рецидива заболевания.
Воспалительные заболевания кишечника в особых случаях
Детский возраст
Состояние хронической болезни приводит к нарушению роста и замедленному половому созреванию. Недостаток школьных и социальных контактов наряду с частыми госпитализациями может иметь важные психологические последствия. Лечение сходное с таковым для взрослых, в некоторых случаях необходимы применение глюкокортикоидов, иммуносупрессоров и хирургическое лечение. Важно проведение мониторинга роста, массы тела и полового развития.
Беременность
Беременность обычно не влияет на активность ВЗК, хотя рецидивы могут встречаться чаще после родов. Медикаментозную терапию, включая аминосалицилаты, глюкокортикоиды и азатиоприн можно без опасений продолжить во время беременности.
Поражения костной ткани
Пациенты с ВЗК склонны к развитию остеопении, остеопороза и переломов. Частично это происходит вследствие использования глюкокортикоидов, и все пациенты, получающие эти препараты более 3 мес, должны также получать бифосфонаты.
Мне уже лучше. Можно ли прекратить лечение? Почему поддерживающая терапия важна для предотвращения обострений болезни Крона
Можно ли прекратить лечение?
Важно понимать, что, хотя вы и чувствуете себя лучше благодаря назначенным вам лекарствам, мы не излечили вас от БК. В настоящее время мы только контролируем это заболевание. Пока мы знаем, что случится, если прекратить лечение БК. Однако то, что мы знаем, указывает на высокую вероятность возврата заболевания, если вы перестанете получать препарат:?: Хотя до начала обострения может пройти год и более, обострение БК разовьется у большинства пациентов, прекративших лечение. Кроме того, когда заболевание вернется, нет никакой уверенности, что вам поможет возобновление прежней терапии. По этой причине вам важно продолжать лечение, оказавшееся эффективным для индукции и поддержания ремиссии.
Причины прекращения терапии
Болезнь Крона и язвенный колит — хронические, протекающие в течение всей жизни заболевания, способ исцеления от которых лекарственными препаратами пока неизвестен. В то же время эффективная терапия иммуносупрессорами стала основой индукции и поддержания ремиссии у больных ВЗК. И для БК, и для ЯК было доказано, что комбинированная терапия тиопуринами и инфликсимабом оказывается более эффективной для достижения клинической и эндоскопической ремиссии, чем применение любого из препаратов по отдельности. Таким образом, эффективное лечение больных ВЗК существует.
Тем не менее пациенты, достигшие ремиссии, как бы мы ее не определяли, часто спрашивают, можно ли отменить и сократить терапию иммуносупрессорами. Вопрос этот возникает в связи со множеством факторов, включая возможность инфекций и злокачественных заболеваний, стоимость препаратов, беременность, лекарственную непереносимость или желание «отдохнуть» от лечения, и не только. Вне сомнения, иммуносупрессоры следует временно отменить при развитии серьезных связанных с ними осложнений. Однако как быть с пациентами, чувствующими себя хорошо и не имеющими осложнений лечения? Безопасно ли отменить или сократить терапию в этой группе больных
Учитывая ограниченность знаний об отмене лекарственной терапии, а также тот факт, что иммуносупрессоры одинаково эффективны при двух этих патологиях, в этой главе будет представлена литература и по ЯК, и по БК.
Уменьшение дозы тиопуринов
Преимущество комбинированной терапии заключается в основном в увеличении остаточного уровня анти-ФНО-препаратов и уменьшении их иммуногенности. Снижение дозы тиопуринов у больных ВЗК, получающих комбинированную или монотерапию, не изучалось. Однако было показано, что повышенный уровень 6-тиогуанина (но не доза тиопуринов) способствует увеличению остаточного уровня инфликсимаба, в связи с чем можно предположить, что при высокой концентрации 6-тиогуанина дозу иммуносупрессора можно сократить.
Уменьшение дозы биологических препаратов
Имеющихся данных недостаточно для того, чтобы судить, безопасно ли уменьшать дозу биологических препаратов у больных ВЗК. В ходе исследования TAXIT уменьшение частоты введений инфликсимаба при повышенной концентрации препарата не привело к изменению частоты ремиссии. У пациентов, достигших клинической ремиссии при еженедельном введении адалимумаба, также изучалось сокращение дозы препарата. Увеличение интервала между введениями адалимумаба с 1 нед до 2 за 6 мес оказалось успешным только у 47 из 75 пациентов (63%). Уменьшать дозу анти-ФНО-препаратов не следует всем пациентам, однако возможность сокращения дозы инфликсимаба можно рассмотреть у больных в клинической ремиссии с повышенным остаточным уровнем препарата.
Прекращение монотерапии иммуномодуляторами
Прекращение терапии иммуномодуляторами (азатиоприном или меркаптопурином) рассматривалось в ходе нескольких исследований как при ЯК, так и при БК. Рандомизированное контролируемое исследование отмены азатиоприна при ЯК показало, что в течение года обострение развивается у 36 и 59% больных, принимающих соответственно азатиоприн и плацебо (p=0,039). Кроме того, в ходе ретроспективного наблюдательного исследования больных с бесстероидной ремиссией ЯК обострения развились приблизительно у 1/3, половины и 2/3 пациентов через соответственно 1, 2 и 3 года наблюдения.
Аналогичное плацебо-контролируемое исследование при БК показало, что через 1, 3 и 5 лет после отмены азатиоприна обострения развиваются соответственно у 14, 53 и 63% больных. Кроме того, схожие данные были получены в ходе масштабного метаанализа, посвященного частоте рецидивов после прекращения монотерапии азатиоприном. В целом у пациентов, успешно получающих иммуномодуляторы, при отсутствии серьезных побочных эффектов или противопоказаний следует продолжать терапию.
Прекращение монотерапии биологическими препаратами
На настоящий момент рандомизированные плацебо-контролируемые исследования по прекращению монотерапии анти-ФНО-препаратами не проводились. Тем не менее, как следует из клинических исследований, проводившихся для оценки эффективности анти-ФНО-терапии, больные, рандомизированные в группу плацебо после индукционного курса, существенно чаще испытывали рецидивы заболевания по сравнению с теми, кому была продолжена анти-ФНО-терапия. По этой причине рекомендуется продолжать поддерживающую монотерапию анти-ФНО-препаратами при ее эффективности и переносимости.
Прекращение терапии иммуномодуляторами, продолжение биологической терапии
Специально для изучения возможности прекращения приема иммуномодулятора и продолжения терапии инфликсимабом было проведено рандомизированное исследование 80 пациентов с не менее чем 6-месячной клинической ремиссией. По сравнению с больными, которым продолжалась терапия иммуномодулятором, в группе, в которой иммуномодулятор отменили, отмечались сравнительное снижение остаточного уровня инфликсимаба и повышение уровня С-реактивного белка. Кроме того, имеются результаты исследования предикторов неэффективности инфликсимаба после отмены азатиоприна у больных с 6-месячной ремиссией БК. В нем было показано, что вероятность эффективности терапии инфликсимабом составляет 85% через 12 мес и 41% через 24 мес. Предикторами неэффективности инфликсимаба были: продолжительность одновременного применения инфликсимаба и азатиоприна (<811 дней), уровень С-реактивного белка >5 мг/л и уровень тромбоцитов >298х109/л. Отменять иммуномодулятор у пациентов, получающих эффективную комбинированную терапию, следует с большой осторожностью. Предпринимать такую попытку, вне сомнения, следует только у пациентов с длительной ремиссией при отсутствии повышенного уровня маркеров воспаления.
Прекращение биологической терапии, продолжение терапии иммуномодуляторами
Исследование группы GETAID было посвящено отмене анти-ФНО-терапии при гормонозависимой БК у пациентов, получающих комбинированную терапию с азатиоприном. Пациенты проходили индукционный курс инфликсимаба (введения на неделе 0, 2 и 6) одновременно с азатиоприном. Затем больные получали только азатиоприн. В результате ремиссия через 12 нед после начала индукции была достигнута у 75% больных, однако это значение сократилось до 57 и 40% через соответственно 24 и 52 нед. В недавно проведенном проспективном когортном исследовании (STORI) изучалась отмена инфликсимаба в группе пациентов с бесстероидной ремиссией БК в течение не менее чем 6 мес комбинированной терапии азатиоприном и инфликсимабом. Из 115 пациентов в течение 1-го года обострение развилось у 44%, а в течение 2 лет — у 52%. К факторам риска, прогнозирующим обострение, были отнесены мужской пол, отсутствие операций в анамнезе, уровень лейкоцитов >6,0х109/л, уровень гемоглобина <145 г/л, уровень С-реактивного белка >5,0 мг/л и уровень фекального кальпротектина >300 мкг/г. Риск обострения существенно снижается у больных с полным заживлением слизистой оболочки по данным эндоскопии. Отмена инфликсимаба изучалась также в ходе ретроспективного исследования у больных ВЗК, включавшего 87% пациентов, дополнительно получавших иммуномодуляторы. К концу 1-го года наблюдения ремиссия отмечалась только у 61% пациентов с БК и у 75% больных ЯК, при этом в течение 10 лет ремиссия сохранилась лишь у 12% пациентов с БК,а при ЯК — у40% больных при 4,5-летнем наблюдении. К другом ретроспективном исследовании, посвященном отмене инфликсимаба (73% больных также получали иммуномодуляторы), была выявлена 35% частота обострений в течение 1 года. Наконец, при проспективном наблюдении 121 пациента с БК после отмены анти-ФНО-препарата, вне зависимости от приема ими тиопуринов, у 45% больных развился рецидив заболевания. Таким образом, следует предостеречь от прекращения анти-ФНО-терапии у больных с ремиссией БК, оставив такую возможность лишь для исключительных случаев, при этом убедившись, что у пациента нет объективных признаков активности заболевания.
Выводы
Важно помнить, что, хотя пациентам с БК и доступна чрезвычайно эффективная терапия, мы не излечиваем их, а лишь сдерживаем хроническое, протекающее всю жизнь заболевание. Хотя подгруппа пациентов с только достигнутой или глубокой ремиссией, которым можно успешно отменить лечение, может быть, и существует, мы не можем заранее с уверенностью выявить таких больных. Хотя отсутствие объективных серологических, эндоскопических и гистологических признаков заболевания может свидетельствовать о том, что терапию можно безопасно сократить, доказательной базы для такой тактики в повседневной клинической практике пока мало.
Варианты лечения резистентной болезни Крона
Как было недавно установлено, при лечении БК без применения биологических препаратов, мы не добиваемся наиболее эффективной индукции и поддержания ремиссии. Если вам в связи с БК еще не назначена биологическая терапия, об этом стоит подумать. Если вы только начали лечение биологическими препаратами, для достижения эффекта требуется время. Клиническое улучшение должно появиться в течение 2-4 нед, но для получения максимального эффекта может понадобиться до 3 мес. Также крайне важно прекратить табакокурение, поскольку оно приводит к ухудшению течения заболевания и уменьшению ответа на биологическую терапию. Исследования показывают, что, продолжая курить, вы в 3 раза увеличиваете вероятность того, что биологическая терапия перестанет вам помогать.
Также следует исключить другие причины, по которым вам может не помогать лечение. К ним относятся инфекции, которым вы становитесь подвержены из-за БК и/или текущего лечения. Их называют оппортунистическими инфекциями, т.е. инфекциями, редко или никогда не появляющимися при обычных обстоятельствах. Впечатление, что лечение не работает, могут создавать и иные причины, не связанные с инфекцией или воспалением. Это может быть стриктура или рубцовое сужение тонкой кишки, изменения кишки из-за операции или даже разрастание бактерий в тонкой кишке. Прежде чем утверждать, что лечение не помогло, следует провести дополнительное обследование. Оно может включить лабораторные анализы, илеоколоноскопию и/или лучевую диагностику. При отсутствии указанных возможных причин мы обсудим возможность добавления второго лекарства — иммуномодулятора или проверим уровень препарата, если вы уже его принимаете, чтобы убедиться, что доза достаточна. После этих мероприятий, выяснив, что лечение действительно неэффективно, может потребоваться назначение препарата этого же класса, но с другим способом введения, или лекарства с иным механизмом действия.
Одной из наиболее волнующих гастроэнтеролога, занимающегося лечением БК, ситуаций является заявление пациента, что «лекарства не помогают». При лечении этого заболевания особенно важно установить взаимоотношения с пациентом, при которых получается обмениваться информацией, пациент не боится рассказать правду о своих тревогах, стрессе, финансовых трудностях и активно описывать текущее состояние болезни. Без этих сведений трудно оценить общее состояние, активность заболевания или неэффективность лечения.
Несмотря на научный прогресс в лечении, варианты которого недавно включили и биологическую терапию, приходится помнить, что приблизительно 1/3 пациентов не ответят на анти-ФНО-терапию. Ситуация, при которой препарат был назначен, но не получен ответ, обозначается как первичная неэффективность. Если же после исходного ответа эффект от лечения был утрачен или развилась непереносимость лечения, диагностируют вторичную неэффективность. Последняя ситуация развивается в 30-40% случаев в 1-й год лечения. Другим удивительным фактом является то, что среди всех пациентов, которые в итоге по разным причинам не ответили на лечение, 2/3 потеряли ответ в первые 12 мес терапии. Хотя эти цифры и отражают общеизвестное развитие заболевания, нам, врачам, следует выработать тактику лечения таких больных. Грамотный выбор и, при необходимости своевременное изменение терапии улучшают результат лечения, повышая качество жизни и уменьшая вероятность операции и госпитализации. Прежде чем констатировать отсутствие ответа у больного, важно в этом убедиться. Некоторые больные могут быть отнесены к резистентным, однако «неэффективность» лечения может быть и не связана с ВЗК. Причиной этого могут быть нераспознанные осложнения заболевания, включая структурные изменения, сопутствующая инфекция или абсцесс или даже симптомы, не связанные с воспалением, такие как СРК.
Нам, клиницистам, полезно придерживаться стандартного алгоритма действий при изменении течения БК, заставляющем подозревать отсутствие ответа. Первым и самым важным состоянием, нередко легко поддающимся лечению, является сопутствующая инфекция, имитирующая отсутствие ответа. Вне зависимости от терапии иммуномодуляторами или биологическими препаратами, наши больные подвержены риску вирусных, бактериальных, паразитарных и грибковых инфекций. Всегда следует исключить Clostridium difficile или другие инфекции, представляющие угрозу для пациента, например цитомегаловирусная инфекция. На риск влияют возраст, анамнез вакцинации, прием антибиотиков или недавние поездки.
Возможные механизмы ухудшения состояния на фоне терапии ингибиторами фактора некроза опухоли
Низкий уровень препарата + подтвержденное воспаление
- Потеря активности анти-ФНО-препарата в связи с образованием к нему антител
- Непрекращающееся воспаление, приводящее к «расходованию» всех анти-ФНО-антител
- Несоблюдение предписаний по лечению
- Потеря активности анти-ФНО-препарата в связи с неиммунным выведением препарата
Достаточный уровень препарата + признаки воспаления
- Изменение патогенетического пути заболевания от опосредованного ФНО к пути, связанному с другими медиаторами
- Инфекция
- Другие причины (васкулит, ишемия)
Достаточный уровень препарата, отсутствие воспаления
- Фибростенозирующая стриктура
- Рак
- СРК
- Различные причины (амилоидоз, избыточный бактериальный рост, диарея, связанная с желчными кислотами, целиакия и др.)
Помимо исключения оппортунистической инфекции чрезвычайно важно также оценить воспаление, равно как и определить уровень препаратов, принимаемых пациентом в данный момент. Концентрация лекарственного вещества в сочетании с воспалительными маркерами дает ценную информацию о том, что вызывает текущие проявления, напоминающие неэффективность терапии.
Приступая к лабораторным исследованиям, следует оценить объективные показатели, такие как С-реактивный белок и фекальные биомаркеры, подтвердившие свою эффективность в оценке воспаления. На рынке доступны два фекальных биомаркера — кальпротектин и лактоферрин. Фекальные биомаркеры полезны в качестве вспомогательного диагностического инструмента, применяемого для мониторинга активности и прогнозирования обострения воспалительного заболевания. Определение этих показателей в ключевые моменты лечения, при установлении диагноза или в начале терапии может предоставить ценную информацию. После того как получены результаты анализа на воспаление, их можно соотнести с уровнем препарата, что позволяет досконально оценить активность заболевания, дозировку препарата и даже соблюдение врачебных предписаний пациентом. Констатируя неэффективность или ускользание эффекта от лечения, необходимо сопоставить эти данные с клиническим рассуждением и, при необходимости, радиологическим и/или эндоскопическим исследованием.
При лечении анти-ФНО-препаратами важно выявить и правильно оценить недостаточный ответ или потерю ответа на биологический препарат, избежав, таким образом, осложнений из-за неполноценного лечения. Чтобы узнать причину явления, прежде чем увеличить дозу, сменить препарат или определить уровень лекарства в крови, сперва нам необходимо решить, имеется ли воспаление. После этого пациента можно отнести к одной из следующих групп:
- с низким уровнем препарата;
- достаточным уровнем препарата и увеличенными биомаркерами воспаления;
- достаточным уровнем препарата и нормальным уровнем биомаркеров.
У пациентов с низким уровнем препарата в первую очередь следует убедиться в соблюдении схемы лечения. К снижению уровня препарата также может приводить высокая активность воспаления или выведение препарата за счет антител к лекарственному средству. На этом этапе для решения вопроса о дальнейшей терапии важно проверить уровень антител к лекарственному средству.
Если у больного выявляется достаточный уровень препарата и высокий уровень биомаркеров воспаления, это может свидетельствовать об изменении патогенетического пути заболевания в сторону не ФНО, а других цитокинов. Это также может свидетельствовать о другом патологическом процессе, например об инфекции, васкулите или ишемии.
Остаются пациенты с нормальным уровнем биомаркеров и достаточным уровнем препарата. У таких больных могут обнаруживаться какие-либо не связанные с воспалением осложнения БК, включая фибростенотическую стриктуру, СРК, опухоль, билиарную диарею, синдром избыточного бактериального роста или даже отложения амилоида.
Основываясь на перечисленных группах больных, нам нужно четко отнести нашего больного к одной из них. В зависимости от разновидности ситуации могут потребоваться дополнительные исследования. Они могут включать илеоколоноскопию, КТ/МРТ или видеокапсульное исследование. Капсульная эндоскопия, как было показано, превосходит все остальные методы исследования при диагностике БК тонкой кишки. Важно помнить, что капсула может застрять при наличии стриктуры. С целью предугадать это осложнение до приема рабочей капсулы применяют пробную капсулу (торговая марка Agile).
Следует помнить, что главное в лечении потери ответа — это его профилактика. Мы добиваемся этого, избегая нерегулярного введения препаратов и обеспечивая достаточный его уровень в крови. Таким образом, мы можем сохранить необходимую концентрацию лекарства в крови и минимизировать образование антител.
Если у пациента действительно развилась потеря ответа, варианты лечения включают: подключение иммуносупрессоров, увеличение дозы текущего анти-ФНО-препарата или его замену на другое лекарственное средство с таким же или иным механизмом действия.
Подключение иммуномодулятора может уменьшить иммуногенность и восстановить эффективность. Следует помнить, что пациенты, принимающие иммуномодуляторы, такие как меркаптопурин или азатиоприн, должны проверяться на уровень метаболитов: 6-тиогуанина и 6-метилмеркаптопурина, чтобы оптимизировать исход лечения и сократить частоту побочных эффектов.
Увеличение дозы или учащение введения может вернуть утраченный ответ на лечение за счет достижения достаточного уровня препарата, соответствующего воспалительной активности. Этого можно добиться за счет учащения введений или увеличения дозы соответствующего препарата. Эффективны оба способа. При получении желаемого ответа можно сократить дозу или частоту введений препаратов.
Если потеря ответа подтвердилась, но ни один из перечисленных способов лечения не помог, может потребоваться назначение препарата с механизмом действия, не связанным с ФНО, или перевод пациента в клинику, где проводятся клинические испытания.
В целом, сталкиваясь с пациентом, утверждающим на приеме, что лекарства ему не помогают, чрезвычайно важно в первую очередь знать вашего больного и быть способным принять взвешенное решение, основываясь на истории заболевания и объективных данных. Надлежащее объективное обследование может включать определение уровня препарата, показателей воспаления, лучевые методы исследования и/или илеоколоноскопию.
Помните:
- необходимо установить причину потери ответа;
- спросить: «Связана ли она с активностью болезни Крона?»
