Врожденные пороки сердца у детей, лечение, причины, симптомы, признаки
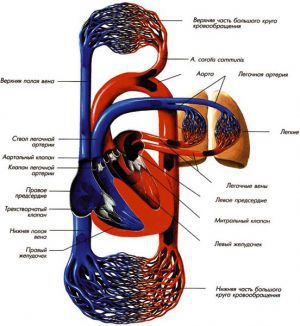
Врожденные пороки сердца.
Причины врожденных пороков сердца
Существует множество разнообразных причин возникновения врожденных пороков сердца (ВПС). Все они в комплексе воздействуют на организм беременной женщины, нарушая процессы формирования органов и систем плода. Сезонные колебания возникновения врожденных пороков сердца главным образом связаны с вирусными эпидемиями. В частности, точно доказано тератогенное (т. е. вызывающее пороки развития) действие на плод вируса краснухи, цитомегаловирусной инфекции, ветряной оспы. Есть данные такого же характера на вирусы гриппа, особенно если заболевание приходится на первые три месяца беременности. Безусловно, наличие только лишь вирусного фактора для развития врожденных пороков сердца сомнительно. Однако при сочетании нескольких тератогенных факторов риск развития врожденных пороков сердца увеличивается. Вирусный агент может стать лишь пусковым механизмом в реализации генетических механизмов. Определенную роль в формировании врожденных пороков сердца отводиться употреблению алкоголя во время беременности, и речь идет не только об крепком алкоголе, но и слабоалкогольных коктейлях, тониках и др. У женщин, потребляющих алкогольные напитки, в 50 % случаев рождаются дети с врожденными пороками сердца. Большая роль во время беременности отводится общему соматическому здоровью женщины. У женщин, страдающих системными заболеваниями (например, системная красная волчанка), сахарным диабетом, чаще рождаются дети с врожденными пороками сердца.
Особое значение имеют лекарственные препараты во время беременности. В частности, в настоящее время доказано тератогенное действие талидомила, препарата, который не только вызывает врожденные пороки сердца, но и другие многочисленные врожденные уродства. Выраженным тератогенным действием обладают амфетамины (вызывают дефект межжелудочковой перегородки и транспозицию магистральных сосудов), противосудорожный препарат гидантоин (приводит к открытому артериальному протоку, стенозу легочной артерии, коарктации аорты), препараты на основе лития (вызывают аномалию Эбштейна, атрезию трехстворчатого клапана), оральные контрацептивные препараты, содержащие прогестагены (вызывают тетраду Фалло и другие сложные врожденные пороки сердца).
Ионизирующее облучение во время беременности зачастую ассоциируется с повышенным риском врожденных пороков сердца. Несомненным фактором риска возникновения врожденных пороков сердца является наследственная предрасположенность. Считается, чем тяжелее порок сердца, тем выше риск повторения врожденных пороков сердца у родственников. Немаловажными факторами для врожденных пороков сердца являются возраст родителей (риск врожденных пороков сердца увеличивается, если мать рожает ребенка в возрасте старше 35 лет), ранние и поздние токсикозы беременности, наличие других детей с врожденными аномалиями внутренних органов. В настоящее время доказано, что немаловажным фактором является состояние здоровья отца.
Основная точка зрения современной кардиологии, объясняющая формирование врожденных пороков сердца, — взаимодействие генетических и средовых факторов, приводящих к нарушению анатомических структур сердца. Хромосомные аберрации регистрируют примерно у 10% пациентов с врожденными пороками сердца.
Патофизиология врожденных пороков сердца
Врач сталкивается с клиническими проблемами больного с врожденными пороками сердца в зрелом возрасте. Так, пороки со сбросом крови слева направо приводят к легочной гипертензии на 3-4-м десятилетии жизни, на десятилетие позже двухстворчатый аортальный клапан приводит к манифестации аортального стеноза. Несмотря на разнообразие врожденных дефектов, некоторые симптомы носят универсальный характер, их встречают у абсолютного большинства больных с врожденными пороками сердца.
Легочная гипертензия (ЛГ) — составная часть практически всех врожденных пороков сердца. Развитие ее приводит к появлению жалоб на резкое снижение толерантности к физической нагрузке, выраженную одышку, образованию асцита. Степень ЛГ — прогностический фактор, определяющий целесообразность хирургического лечения, качество и продолжительность жизни больного. К ЛГ в первую очередь приводит резкое увеличение объема крови через легочную артерию, что всегда возникает при сбросе крови слева направо. Вторая причина ЛГ — значительный рост сосудистого сопротивления. Патогенез поражения легочных сосудов остается неясным. Четко установлено, что по мере нарастания легочной гипертензии прогрессирует обструкция и пролиферация легочных артериол, тонус артерий повышен. Сочетание спазма сосудов с их морфологической перестройкой приводит к выраженному шунтированию крови в легких, с быстрым развитием гипоксемии, ишемии тканей, изменением рН тканей в сторону ацидоза. Это еще более усиливает шунтирование крови за счет спазма прекапилляров и ухудшения микроциркуляции. Нарастание легочной гипертензии носит необратимый характер и со временем уровень давления в легочной артерии становится настолько высоким, что возникает принципиально новая внутрисердечная гемодинамика — сброс справа налево.
Гипоксемия стимулирует синтез эритропоэтина, что, в свою очередь, стимулирует синтез эритроцитов. Увеличенное число эритроцитов — эритроцито; — может быть как компенсированным, так и декомпенсированным. Компенсированный эритроцитоз характеризуется уровнем гематокрита, не превышающим 65%, отсутствием синдрома повышенной вязкости крови, нормальным содержанием железа в сыворотке крови. Декомпенсированный эритроцитоз характеризуется более высоким уровнем гематокрита и гипервязкостью крови. Кровопускание долгий период времени рассматривали как единственный способ коррекции декомпенсированного эритроцитоза. Компенсированный эритроцитоз не требует коррекции кровопусканием. В последние годы пришло понимание того, что кровопускание, принося временное облегчение, приводит к быстро нарастающему дефициту железа, который, в свою очередь, приводит к нарастанию пула микроцитов. Микроциты обладают низкой способностью к прохождению через микроциркулятор-ное русло и повышают вязкость крови. Низкая способность микроцитов к транспорту кислорода усугубляет гипоксию тканей.
Синдром гипервязкости крови вызывает повышенное тромбоцитообразование и тромбоэмболию. Ряд препаратов, и в первую очередь пероральные контрацептивы, резко повышают риск тромбообразования у этих больных. Второй фактор, усугубляющий течение болезни при эритроцитозе, — обезвоживание организма. В связи с этим сниженный диурез может провоцировать тромбоз и тромбоэмболический синдром. Выбор ежедневной дозы мочегонных — предмет особого внимания врача и требует ежедневного учета объема выпитой жидкости и выделенной мочи.
Классификация врожденных пороков сердца
Простой и легко определяемый критерий, позволяющий разделить все врожденные пороки сердца на 2 группы, — цианоз. По наличию или отсутствию цианоза выделяют нецианотические и цианотические пороки. Нецианотические пороки бывают со сбросом слева направо и без сброса.
Нецианотические пороки со сбросом крови слева направо — пороки со сбросом крови на уровне предсердий (дефект межпредсердной перегородки), на уровне желудочков (дефект межжелудочковой перегородки), на уровне корня аорты (из корня аорты в правый желудочек или в легочную артерию).
Нецианотические пороки без сброса — пороки правых отделов сердца (аномалия Эбштейна, стеноз легочных вен, изолированное расширение легочного ствола) и пороки левых отделов сердца.
Цианотические пороки — пороки с повышенным легочным кровотоком и с нормальным легочным кровотоком.
Повышенный легочный кровоток возникает при отхождении аорты и легочной артерии от правого желудочка, общем аортолегочном стволе, общем предсердии, тетраде Фалло.
Нормальный легочный кровоток сохраняется при синдроме Эбштейна, отхождении аорты и легочной артерии от правого желудочка + стеноз легочной артерии, атрезии трехстворчатого клапана.
Врожденные пороки сердца, подобно другим аномалиям развития, как установлено в последние годы, нередко представляют собой следствие инфекций, особенно вирусных, перенесенных матерью в первые месяцы беременности (например, краснухи).
Развитие некоторых дефектов строения тела при врожденном сифилисе известно уже давно.
Распознаванию врожденных пороков, помимо анамнеза, особенно способствует наличие:
- резкого цианоза и «барабанных пальцев»;
- грубого систолического «машинного» шума и дрожания в области II—IV ребра слева;
- резкого выбухания дуги легочной артерии и правограммы при электрокардиографическом исследовании.
В 1/3 случаев врожденные пороки осложняются ревматическим вальвулитом—ревматическим пороком и приблизительно так же часто под-острым септическим эндокардитом.
Ниже приводится только краткое описание наиболее частых врожденных пороков сердца.
Группа врожденных пороков сердца без цианоза (или лишь с поздним цианозом при декомпенсации сердца)
1. Незаращение боталлова протокa (ductus Botalli apertus). По боталлову протоку в утробной жизни, пока еще нет легочного дыхания, кровь из легочной артерии, минуя легочный круг и левый желудочек, проходит прямо в аорту и, далее, в тело плода. После рождения ребенка, когда он начинает дышать, расправляется легочная кровеносная сеть, проток закрывается, возможно в результате первоначального мышечного спазма, и тромбируется.
В случае незаращения протока сохранение прямого сообщения между аортой и легочной артерией усложняет кровообращение. Кровь из аорты при сокращении левого желудочка (где давление выше, чем в легочной артерии) частично выбрасывается через проток в легочную артерию. Чтобы обеспечить нормальное снабжение периферии артериальной кровью, левый желудочек должен выбрасывать больше крови, вследствие чего он расширяется и гипертрофируется. Избыточное поступление крови в легочную артерию приводит к растягиванию ее и перегрузке правого желудочка, который также гипертрофируется. Часть крови непроизводительно циркулирует из аорты в легочную артерию и обратно в левый желудочек.
Наиболее характерен громкий двойной непрерывный «машинный» шум во втором левом межреберье, проводящийся и насквозь к спине; во время систолы кровь под большим давлением с вибрацией стенки—«кошачьим мурлыканьем» — выбрасывается в легочную артерию, вследствие чего и второй тон легочной артерии усилен; во время диастолы, когда давление в аорте падает, кровь возвращается частично из растянутой легочной артерии обратно в аорту; при меньшем дефекте во время диастолы шума не слышно. Определяется приглушение во втором и третьем межреберье слева за счет расширения conus pulmoualis и легочной артерии.
Верхушечный толчок усилен, сердце расширено влево. Влево от грудины определяется диффузная пульсация правого желудочка и пульсаторные толчки в области легочной артерии. Рентгенологически обнаруживается выступание дуги легочной артерии; сердце расширено влево за счет обоих желудочков, с усилением пульсации левого края и больших сосудов, особенно легочной артерии; могут пульсировать и крупные разветвления легочной артерия в воротах легких («пляска гилюсов»). Резкая пульсация, указывающая на перебрасывание большого количества крови, может сопровождаться лишь слабым шумом, что подчеркивает большое значение рентгенологического исследования для оценки величины дефекта. На лучевой артерии нерезко выраженный pulsus celer с пульсовым давлением, увеличенным соответственно степени зиянии протока. Электрокардиограмма большей частью показывает отклонение оси вправо. Возвращение боталлова протока наблюдается чаще у женщин.
Для предотвращения наиболее опасного септического эндокардита—рекомендуют делать операцию перевязки или рассечения протока.
2. Дефект межжелудочковой перегородки болезнь Толочинова-Рожо.Дефект локализуется ближе к фиброзной части перегородки, тотчас под устьем аорты, вызывает во время систолы непроизводительное выбрасывание из левого желудочка в правый части крови, возвращающейся через легочный круг в левое сердце; отсюда—длинный грубый систолический шум над сердцем, особенно в середине грудины, у IV реберного хряща слова, часто вместе с вибрацией стенки. Через меньший дефект кровь проходит с большим шумом. Расширены и гипертрофированы оба желудочка, выбухает легочная дуга, верхушечный толчок усилен. При малом дефекте изменения контура сердца и шум незначительны. Пороку сопутствует врожденная легко переносимая атриовентрикулярная блокада, если вовлечен и пучок Гиса, проходящий за фиброзной частью межжолудочковой перегородки.
Если дефект перегородки сопровождается другой врожденной аномалией или застоем крови в легких, а вместе с тем давление в правом желудочке превышает давление в левом сердце, то кровь (венозная!) перебрасывается из правого желудочка в левый и наступает цианоз.
Незаращение овального отверстия (foramen ovale apertum) часто клинически ничем не проявляется, за исключением парадоксальных эмболии из вен большого круга прямо в аорту и артерии большого круга.
3. Стеноз перешейка аорты (stenosis isthmus aorlae, coarctatio aortae) образуется за счет тяжей ниже места отхождения левой подключичной артерии, вследствие чего давление в аорте, бедренных артериях, почечных и других ниже места стеноза падает, а выше этого моста— нарастает; левый желудочек гипертрофируется. Верхушечный толчок усилен. Часто выслушивается систолический шум у основания сердца или между лопатками слева. На рентгенограмме восходящая аорта расширена и удлинена, выступ ее отсутствует. Кровоснабжение обеспечивается расширенными, извитыми, резко пульсирующими коллатералями из ветвей подключичной и внутренней грудной (a. mammaria interna) артерий через межреберные артерии (их расширение дает характерные узуры ребер, видимые на рентгенограмме) и поверхностные аа. epigastricae. Все же возможно похолодание стоп, перемежающаяся хромота, даже отставание развития нижней половины тела.
Группа врожденных пороков сердца о ранним цианозом (синяя болезнь; morbus eoerulcns)
Лица, у которых с детства наблюдается ранний цианоз, пальцы наподобие барабанных палочек, эритроцитоз, увеличение массы крови (и в период, когда еще нет слабости миокарда), почти всегда относятся к так называемой тетралогии Фалло. Это—сложная аномалия, когда имеется одновременно стеноз устья легочной артерии, приводящий к повышению давления в правом желудочке, декстропозиция аорты, при которой венозная кровь поступает в аорту прямо из правого желудочка, незаращение межжелудочковой перегородки и резкое расширение правого желудочка.
Над легочной артерией определяется систолический шум и дрожание, резкое расширение правого желудочка, правограмма на электрокардиограмме. Работоспособность может быть отчасти сохранена.
Другие врожденные дефекты также могут вызывать постоянный цианоз.
Декстрокардия (dextrocardia)
Порок развития с извращением (как бы зеркальным отображением) расположения сердца и больших сосудов пли также и всех внутренних органов (situs viscerum inversus) сразу распознается при рентгеноскопии, но нередко просматривается при обычном физическом исследовании больных. Электрокардиограмма в нервом отведении извращена; третье отведение соответствует второму нормальному (имеет наибольшие зубцы). Аномалия не имеет клинического значения, однако нередко декстрокардия сочетается с другими более серьезными врожденными пороками сердца; в случае обратного расположения брюшных внутренностей могут возникнуть затруднения при распознавании аппендицита и т. д.
Нередко за врожденную аномалию принимают резкое смещение сердца вправо при в результате слипчивого плеврита и т. д.
(dextropositio cordis), правильно распознать которое можно на основании анамнеза, западения и ограничения подвижности половины грудной стенки, плевральных сращений на рентгенограмме, нормальной в общих чертах электрокардиограммы и т. д.
Врожденные пороки сердца у взрослых
Несмотря на впечатляющие успехи медицины в последние десятилетия, проблема врожденных пороков сердца остается актуальной. Статистический анализ числа новорожденных с врожденными пороками в 30-е, 60-е и 80-е годы прошлого века показывает, что их число остается стабильным. С пороками сердца рождаются 0,8-1,0% детей. Внедрение новых методов своевременной диагностики пороков и успехи хирургии позволяют существенно продлить жизнь детей с врожденными пороками сердца и увеличить их долю среди взрослого населения. До 1938 г. практически любой врожденный порок рассматривался как абсолютно неизлечимое заболевание, приводящее к летальному исходу в раннем детстве или существенно сокращающее продолжительность жизни до 10-30 лет. В 1938 г. R. Cross выполнил первое шунтирование легочной артерии — начало эры хирургического лечения врожденных пороков сердца. Выдающийся успех хирургического метода лечения врожденных пороков сердца продемонстрировал в 1959 г. W. Lillihei, впервые выполнивший коррекцию тетрады Фалло. В конце 1960-х годов разработана хирургическая коррекция транспозиции магистральных артерий и дефектов межжелудочковой перегородки. Широкое внедрение хирургической коррекции пороков привело к значимому увеличению числа больных с тетрадой Фалло, доживших до старших возрастных групп. По данным амбулаторной службы США, ежегодно рождаются примерно 32 000 детей с врожденными пороками сердца. В течение 1 -го года жизни умирают 20% из них. Этот уровень, достигнутый в 2000 г. на 40% ниже, чем аналогичный показатель 1960 г. Ежегодно выполняют до 20 000 операций, подростковый период переживают 80% оперированных детей. В 1985— 1990 гг. в США жили 300 000 взрослых с врожденными пороками, а в 2000 г. — 900 000 взрослых, что наглядно показывает рост числа взрослых пациентов с врожденными пороками в современном мире, находящихся в сфере ответственности здравоохранения.
Ведущее направление в мировой практике наблюдения за больными с врожденными пороками сердца — создание мультидисциплинарных центров. Однако для значительного числа таких пациентов решение вопросов, связанных с состоянием их здоровья, по-прежнему принадлежит врачу.
Лечение
- Необходима консультация специалиста. Чтобы получить представление о заболевании, требуется детальная оценка гемодинамических показателей, включая электрофизиологическое исследование. Одним из наиболее важных терапевтических вмешательств может быть коррекция какой-либо послеоперационной гемодинамической аномалии, лежащей в основе аритмии.
- Регистрируют ЭКГ в 12 отведениях.
- Во время регистрации ЭКГ вводят аденозин внутривенно. Способ прекращения тахиаритмии может дать полезную информацию о ее этиологии, например предвозбуждение.
- Неотложная кардиоверсия может потребоваться при ухудшении гемодинамических показателей. В идеале чреспищеводная ЭхоКГ должна исключать интракардиальное тромбообразование. Если пациент принимает варфарин, перед кардиоверсией всегда нужно проверять MHO и концентрацию электролитов в сыворотке крови.
Женщины с врожденными пороками сердца, которым противопоказана беременность
- Легочная гипертензия, например при синдроме Айзенменгера (50% случаев материнской смерти и смерти плода; смерть матери может наступить в течение двух недель после родов).
- Сердечная недостаточность, вторичная к недостаточности кровообращения Фонтана.
- Женщины с выраженным цианозом и полицитемией:
- Если насыщение кислородом менее 80% в покое и уровень гемоглобина более 180 г/л, существует высокая вероятность выкидыша или внутриутробной задержки развития.
Дефект межпредсердной перегородки
Один из наиболее распространенных пороков, проявляющийся впервые во взрослой жизни. Обычно остается незамеченным из-за того, что стойкое расщепление второго тона сердца достаточно трудно выслушать. ДМПП может проявиться в виде вновь возникшего приступа трепетания предсердий или ФП. Следует рассмотреть необходимость электрофизиологического вмешательства, например операцию «лабиринт» при фибрилляции предсердий. Сброс крови имеет склонность к нарастанию с возрастом, так как левый желудочек теряет эластичность. Устранение порока показано всем пациентам с симптомами ДМПП и некоторым пациентам без симптомов — по результатам сердечно-легочного тестирования. Возрастных ограничений не существует. Большинство дефектов вторичного отверстия подлежат транскатетерному устранению. Должна быть исключена легочная гипертензия. Предсердные аритмии являются одной из наиболее распространенных проблем в медицине в последнее время. Все остальные виды дефектов: дефект венозного синуса (дефект верхнего отдела межпредсердной перегородки, связанный с «сидящей верхом» верхней полой веной и аномальным оттоком из правых легочных вен) и частичный дефект атриовентрикулярной перегородки — требуют хирургического вмешательства. Устранение дефекта венозного синуса, связанное с перенаправлением аномальных легочных вен, представляет наибольшую сложность для хирургов. Риск развития эндокардита очень низок. Профилактика антибиотиками не показана.
Дефект межжелудочковой перегородки
Большинство дефектов имеют небольшой размер и устраняются еще в детстве. Синдром Айзенменгера (заболевание легочных сосудов, связанное с обратным, справа налево, сбросом крови через внутрипредсердное сообщение) встречается достаточно редко. Показания к закрытию Дефекта: значительный сброс крови, перенесенный эндокардит, развитие недостаточности аортального клапана или обструкция правожелудочковых путей оттока крови. Всегда необходимо выяснить обратимость легочной гипертензии до проведения вмешательства.
Дефект межпредсердной и межжелудочковой перегородки
Характерный дефект у пациентов с синдромом Дауна. Если не сделать операцию, развивается поражение сосудов легких (синдром Айзенменгера). Левожелудочковая клапанная недостаточность или стеноз являются определяющими при рассмотрении необходимости дальнейшей операции. Может понадобиться замена клапана. Всем пациентам показана профилактика эндокардита.
Стеноз клапана легочной артерии
Впервые может проявиться во взрослой жизни. Успешно лечится с помощью баллонной пластики клапана, которую проводят, если на допплер-ЭхоКГ клапанный градиент давления превышает 30 мм рт.ст. Хирургическое лечение применяют при кальцификации и дисплазии клапана. При послеоперационном наблюдении не возникает проблем, риск развития эндокардита низок.
Обструкция левожелудочковых путей оттока крови
Стеноз аортального клапана особенно часто сочетается с двустворчатым клапаном аорты. Это комплексное поражение, которое часто сопровождается поражением стенки аорты. Существует риск расширения и разрыва аорты. Степень стеноза или регургитации могут увеличиваться со временем. Необходимо серьезно рассматривать необходимость вмешательства при низкой переносимости физических нагрузок, боли в грудной клетке или обмороках, особенно при нагрузках. Иногда обструкцию удается устранить с помощью баллонной пластики клапана, но обычно требуется хирургическое вмешательство. Существует два варианта операций: замена аортального клапана (пожизненная антикоагулянтная терапия) и имплантация гомологичного трансплантата или операция Росса (антикоагулянтная терапия не требуется, но существует потенциальная необходимость в повторном вмешательстве). Субаортальный стеноз не так распространен (отсутствует щелчок изгнания) и при тяжелой форме, когда у пациента проявляются симптомы, требует хирургической коррекции. Возможны рецидивы. Надклапанный стеноз обычно наблюдают у пациентов с синдромом Уильямса. Он может быть связан с множественными стенозами устьев коронарных артерий и ветвей дуги аорты. Операция по устранению этого порока достаточно сложная.
Коарктация аорты
Большинство пациентов наблюдают в отделениях для взрослых уже после операции. Впервые коарктация может проявиться гипертензией. При осмотре всегда нужно проверять пульс на бедренной артерии! У женщин обращают внимание на симптом Тернера. Коарктация аорты — сложный порок, обычно сочетающийся с двустворчатым аортальным клапаном (щелчок изгнания на верхушке сердца) и поражением стенки аорты. Во время осмотра измеряют давление на верхней и нижней конечностях, на ЭКГ и двумерной ЭхоКГ отмечают признаки гипертрофии левого желудочка. Со временем может возникнуть повторная коарктация, которую можно спрогнозировать по ослаблению пульсации бедренной артерии и несогласованности пульса на лучевой и бедренной артериях. При допплер-ЭхоКГ можно получить сигнал о возросшей систолической скорости с продолжающимся током крови в месте повторной коарктации в фазу диастолы. Предпочтительно использовать МРТ. У большинства пациентов возможны баллонная дилатация и стентирование, что помогает избежать вероятных осложнений хирургического вмешательства на аорте. Послеоперационное наблюдение необходимо, чтобы исключить образование аневризмы или рецидива. Пациентам показана антибиотико-профилактика.
Аномальный дренаж легочных вен
Многие пациенты переносят операцию в раннем детстве. Иногда ассоциируется с синдромом «ятагана». Если у пациента обнаруживают симптомы (одышка, аритмия) и признаки перегрузки объемом правого желудочка, например, при двумерной ЭхоКГ, пациенту показано хирургическое вмешательство. Риск развития эндокардита низок.
Транспозиция магистральных сосудов
Аорта выходит из правого желудочка, легочной ствол — из левого. Наиболее распространенный цианотический порок, проявляющийся в первые дни жизни. При отсутствии смешения крови на сердечном или артериальном уровне эта патология несовместима с жизнью. Большинство пациентов, доживших до зрелого возраста, перенесли внутрипредсердное устранение порока по Мастерду или Сеннигу. Однако эти операции не могут обеспечить длительной выживаемости. Наиболее распространенными осложнениями в позднем послеоперационном периоде являются предсердные аритмии (трепетание или фибрилляция), сужение венозного просвета и недостаточность правого желудочка с недостаточностью трехстворчатого клапана. Аритмии плохо переносятся, и быстрое восстановление синусового ритма жизненно важно. Стеноз просвета может быть устранен с помощью транскатетерной баллонной дилатации или стентирования. Желудочковая недостаточность требует интенсивной консервативной терапии, но, в конечном итоге, может появиться необходимость в трансплантации сердца. Пациенты, перенесшие операцию по устранению порока, доживают до взрослой жизни; у некоторых отмечают проблемы со стенозированными коронарными артериями и местом реанастомоза новой аорты. Требуется антибиотикопрофилактика.
Тетрада Фалло
Включает непрепятствующий току крови ДМЖП больших размеров, высокое положение аорты, обструкцию правожелудочковых путей оттока крови и гипертрофию правого желудочка. Наиболее распространенный цианотический порок, проявляющийся после неонатального периода. Если в неонатальном периоде развивается выраженный цианоз, ребенку могут провести паллиативное шунтирование Блелока-Тауссиг, а затем и полную репарацию. В некоторых клиниках предпочитают окончательное вмешательство в течение первых месяцев жизни.
Подавляющее большинство взрослых перенесли какую-либо операцию по устранению порока с закрытием дефекта перегородки и ослаблением обструкции правожелудочковых путей оттока крови хирургическим путем. Аритмии являются неизбежным последствием операции (рубцевание, вентрикулотомия и легочная недостаточность). Поздние аритмии (как предсердные, так и желудочковые) могут привести к внезапной смерти. Известно, что легочная недостаточность, игнорируемая многие годы, является одной из наиболее важных причин заболеваемости и смертности у пациентов, перенесших операцию по поводу обструкции правожелудочковых путей оттока крови. Продолжительность комплекса ORS более 180 мс на ЭКГ используют как индикатор риска развития аритмии и поздней внезапной смерти. Состояние пациентов должно быть оценено путем проведения нагрузочных проб и МРТ. На сегодняшний день стала возможной чрескожная имплантация клапана с помощью стента из сплава платины и иридия с использованием клапана яремной вены быка. Операция возможна у пациентов с тяжелой формой недостаточности клапана легочной артерии и диаметром пути оттока крови менее 20 мм. Стеноз ветвей легочных артерий требует агрессивного лечения с помощью катетерного вмешательства. Имплантация гомологичного клапана хирургическим путем выполняется в специализированных центрах с операционной смертностью менее 1%. Большинство таких имплантатов требуют замены через 10 лет, другими словами, требуются повторные операции. Профилактика эндокардита показана всем пациентам.
Пациенты, перенесшие операцию Фонтана
Это окончательная паллиативная операция у пациентов, рожденных с картиной «одного желудочка», в котором венозная кровь из большого круга направляется в легкие без участия «сублегочцого желудочка», например атрезия митрального, трехстворчатого, легочного или аортального клапана. Операция обеспечивает хорошую выживаемость в раннем и среднем послеоперационном периоде, но недостаточность появляется даже у тщательно отобранных пациентов. К поздним проблемам относят предсердные аритмии, включающие дисфункцию синусового узла и атриовентрикулярную блокаду, недостаточность атриовентрикулярного клапана, желудочковую недостаточность, обструкцию вен и энтеропатию, приводящую к потере белка (5-летняя выживаемость менее 50%). Порок Фонтана — наиболее сложная проблема. В этом случае необходима трансплантация или замена на более модернизированную модификацию с сопутствующей операцией по устранению аритмии.
Врожденно-скорректированная транспозиция магистральных сосудов
Цианоз развивается при сопутствующих ДМЖП и стенозе легочного ствола или при заболевании сосудов легких и ДМЖП без стеноза клапана легочной артерии. Это редкий порок с нормальной выживаемостью, если он изолированный. Постоянно существует риск полной атриовентрикулярной блокады (2% в год). Недостаточность атриовентрикулярного клапана, сопровождаемая правожелудочковой недостаточностью, длительное время является наиболее серьезной проблемой.
Аномалия Эбштейна трехстворчатого клапана
Этот порок вызван апикальным смещением трехстворчатого клапана и сообщением между предсердиями. Цианоз возникает из-за сброса крови справа налево на уровне предсердий. Порок имеет широкий спектр проявлений, зависящих от величины недостаточности трехстворчатого клапана и сопутствующих пороков. В младенчестве это проявляется цианозом и сердечной недостаточностью; в этом случае у заболевания плохой прогноз. У старших детей и подростков признаком может быть шум, а легкие формы могут протекать бессимптомно. Распространены предсердные аритмии, вызванные предвозбуждением (дополнительные проводящие пути). Вмешательство проводят у пациентов с симптомными аритмиями, сердечной недостаточностью и тяжелой формой недостаточности трехстворчатого клапана. Может быть осуществлена замена или пластика клапана. Внутрипредсердное сообщение, приводящее к цианозу и парадоксальной эмболии, может быть устранено чрескожно, если позволяют гемодинамические показатели.
Подозрение на врожденный порок сердца у детей
Предварительные замечания
Большинство новорожденных детей с врожденным пороком сердца (ВПС) сразу после рождения бессимптомны.
Критическими периодами являются:
- Период закрытия артериального протока (3—5 дни жизни). У детей с дуктусзависимым легочным или системным кровотоком это приводит к ситуации, требующей экстренного вмешательства!
- Влияние снижающегося легочного сосудистого сопротивления на протяжении первых нескольких недель жизни. При определенных обстоятельствах значительное увеличение объема шунта с развитием легочной гипертензии, напр., при полной форме АВ-коммуникаций, общем артериальном стволе, большом ОАП, аорто-пульмональном окне, сложных пороках с гемодинамически единственным желудочком сердца и т.д.
Анамнестические данные
Семейный анамнез:
- Риск развития ВПС: для всех новорожденных 0,8 %. при наличии родственника 1-й линии с ВПС 3—4 %. при наличии двух родственников 1-й линии с ВПС риск примерно 10 %.
- Кардиомиопатии.
- Синдромы: трисомии 21, делеция 22 хромосомы, синдром Марфана, Нунан, Эллиса ван Крефельда, Хольта-Орама, синдром удлиненного QT, гликогенозы, мукополисахаридозы и др.
Факторы риска со стороны матери:
- Сахарный диабет, фенилкетонурия.
- Коллагенозы (особенно системная красная волчанка как причина врожденной АВ-блокады).
- Злоупотребление алкоголем.
- Прием медикаментов с тератогенным эффектом (противосудорожные препараты, витамин А, литий и др.).
- Инфекции: краснуха, ЦМВ, ВИЧ, вирус Коксаки
- Возраст матери.
Характерные клинические симптомы у новорожденного
Малый размер для гестационного возраста
Шум в сердце: особенно при обструктивных пороках, слышен сразу после рождения.
Клинические проявления сердечной недостаточности: усиленная потливость, тахипноэ, слабость сосания, непереносимость нагрузки, задержка прибавки в весе и росте.
Диагностика
Осмотр:
- Бледно-серый или цианотичный цвет кожного покрова.
- Дыхание учащенное (тахипноэ), глубокое, стонущее.
- Отеки, часто вначале сложно интерпретировать.
- Усиленный сердечный толчок.
- Признаки дисморфизма.
Пальпация:
- Pulsus celer et altus = напр., при ОАП или аортальной недостаточности.
- Pulsus parvus = низкий сердечный выброс на фоне сердечной недостаточности или обструкции левых отделов сердца.
- Разница пульса на верхних и нижних конечностях при коарктации аорты.
- Дрожание грудной клетки, прекордиальная пульсация (эпигастрий = правый желудочек, верхушка сердца = левый желудочек).
- Гепатоспленомегалия.
Аускультация:
- Систолический и/или диастолический шум в сердце, часто выслушиваемый лишь на 3—4 день жизни.
- Единичный, со стойким расщеплением, или пушечный 2 тон сердца.
- Тон изгнания.
- Ритм галопа, аритмии.
Внимание: Шум в сердце может вовсе отсутствовать.
Дальнейшие мероприятия: При наличии данных в пользу ВПС показано проведение эхокардиографии, ЭКГ.
