Дефект межжелудочковой перегородки сердца: что это такое, причины, лечение, симптомы, признаки
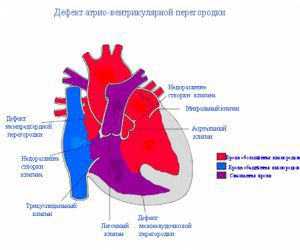
Самая частая локализация дефекта межжелудочковой перегородки — перепончатая часть перегородки (мембранозный дефект) - 80%.
Что такое дефект межжелудочковой перегородки сердца
Врождённый дефект межжелудочковой перегородки (ДМЖП) — результат неполного образования перегородки между желудочками. У эмбриона МЖП состоит из мембранозной и мышечной части. Большинство врождённых дефектов «перимембранозные», т.е. они находятся в месте соединения мембранозной и мышечной части.
Причины дефекта межжелудочковой перегородки сердца
ДМЖП — самые часто встречающиеся ВПС: 1 на 500 детей, родившихся живыми. Дефект может быть изолированным или представлять собой часть сложного ВПС. Приобретённый ДМЖП может произойти при её разрыве, осложнившем острый ИМ, или при травме.
Продолжительность жизни больного определяется состоянием гемодинамики, которая зависит от площади дефекта и состояния легочных артерий. Локализация дефекта оказывает меньшее влияние на прогноз. У больного, дожившего до взрослого возраста и не подвергшегося хирургическому лечению, исходно дефект небольшой. Неоперированный больной со значимым дефектом, как правило, умирает в детском возрасте. МЖП может закрыться спонтанно. Примерно 50% всех дефектов имеет малые размеры, а три четвертых из них закрываются спонтанно. Даже большие по площади дефекты с возрастом уменьшаются. Спонтанно закрываются, как правило, дефекты в трабекулярной части МЖП и очень редко в мембранозной части. Спонтанное закрытие дефектов происходит в первые 5 лет жизни ребенка в 90% всех случаев. В литературе описаны единичные случаи спонтанного закрытия дефекта у взрослого. Таким образом, врач, наблюдающий подростка или взрослого больного с дефектом межжелудочковой перегородки, имеет дело с практически стабильной площадью дефекта. При отсутствии существенных изменений площади дефекта решающая роль в прогнозе заболевания принадлежит легочному сосудистому сопротивлению, степень которого зависит от перегрузки объемом крови, возникающей при сбросе крови слева направо.
Симптомы и признаки дефекта межжелудочковой перегородки
Кровоток из ЛЖ с высоким давлением в ПЖ низким давлением во время систолы продуцирует пансистолический шум, иррадиирующий по всей прекордиальной области. Маленький дефект часто продуцирует громкий шум (maladie de Roger) при отсутствии других нарушений гемодинамики. И наоборот, большой дефект может давать мягкий шум, особенно при увеличении давления в ПЖ.
Врождённый ДМЖП проявляется как СН в младенчестве или как шум с минимальными нарушениями гемодинамики у старших детей и взрослых и редко — как синдром Эйзенменгера. У некоторых детей шум становится тише или исчезает после спонтанного закрытия дефекта.
Сердечная недостаточность осложняет большой дефект обычно в период 4-6 нед жизни, но отсутствует в раннем постнатальном периоде. Помимо шума, имеется выраженная парастерналь-ная пульсация, тахипноэ и втяжение нижних рёбер на вдохе. При рентгенологическом исследовании грудной клетки видно полнокровие лёгких, на ЭКГ — синдром гипертрофии ЛЖ и ПЖ.
Обычно наблюдают в срок от 24 ч (наибольший риск) до 10 сут после ОИМ и встречают в 2-4% случаев. Клинически наблюдается резкое ухудшение состояния пациента, появление грубого пансистолического шума (с эпицентром в области левого края грудины, внизу), нарушение тканевой перфузии и отек легких. Отсутствие шума у пациента с низким сердечным выбросом не исключает дефекта межжелудочковой перегородки.
В клинической практике принято оценивать:
- отношение легочного кровотока к общему кровотоку;
- среднее давление в легочной артерии;
- отношение легочного сосудистого сопротивления к общему сосудистому сопротивлению.
В 1994 г. в рамках клинического исследования «Первая естественная история изучения врожденных пороков сердца» (First Natural History Study of Congenital Heart Defects) создана классификация дефекта межжелудочковой перегородки с учетом величин, характеризующих связь легочного кровотока и легочного сосудистого сопротивления с системным кровотоком и системным сосудистым сопротивлением. В классификации учтен уровень давления в легочной артерии. В соответствии с классификацией все дефекты межжелудочковой перегородки разделены на 4 группы:
- группа 1 — дефект межжелудочковой перегородки с незначительным сбросом крови; отношение легочного кровотока к системному < 1,5, а среднее давление в легочной артерии <20 мм рт.ст.;
- группа 2 — дефект межжелудочковой перегородки с выраженным сбросом крови; отношение легочного кровотока к системному >1,2, среднее давление в легочной артерии повышено (>20 мм рт.ст.); легочное сосудистое сопротивление еще значимо не выросло: отношение легочного сосудистого сопротивления к системному <0,2;
- группа 3 — дефект межжелудочковой перегородки с большим сбросом крови; легочное сосудистое сопротивление растет значительно;
- группа 4 — пациенты с синдромом Эйзенменгера; легочное сосудистое сопротивление достигает 65% системного; давление в легочной артерии практически равно системному давлению.
У больных 1-й группы не развиваются значимые морфофункциональные изменения камер сердца. При выраженном или значимом сбросе крови начинается и быстро прогрессирует морфофункциональная перестройка камер сердца.
- Величина левого предсердия и левого желудочка зависит напрямую от степени и выраженности сброса крови слева направо. Больший объем крови в правом желудочке, возникший из-за суммирования двух объемов из правого предсердия и из левого желудочка, вызывает перегрузку объемом крови легочной артерии, сосудов малого круга и легочных вен, а следовательно, и левого предсердия. Перегрузка объемом крови левого предсердия вызывает повышение в нем давления и его увеличение. Больший объем крови, поступающий из левого предсердия в левый желудочек, приводит к его гипертрофии и дилатации. Следовательно, ремоделирование левых отделов сердца — функция величины сброса слева направо. Примерно у 5% больных с дефектом межжелудочковой перегородки возникает пролабирование створки аортального клапана в дефект межжелудочковой перегородки, которое клинически проявляется аортальной недостаточностью. Такое течение заболевания резко ухудшает прогноз болезни.
- Правый желудочек сердца испытывает перегрузку объемом крови, которая передается в легочную артерию и легочные сосуды и приводит к обструкции и облитерации легочных артериол. Помимо морфологической перестройки легочных артерий, в них возникает выраженный спазм. Суммирование морфологической перестройки легочных артерий и их спазма приводит к резкому росту легочного сосудистого сопротивления и давления в легочной артерии. Таким образом, правый желудочек в систолу преодолевает возросшую постнагрузку, что приводит к его быстрой гипертрофии, дилатации и выраженному росту как конечно-диастолического, так и конечно-систолического давления. Примерно у 5% больных с дефектом межжелудочковой перегородки образуется обструкция выносного тракта правого желудочка.
При декомпенсации функции правого желудочка в процесс включаются трикуспидальный клапан и правое предсердие. Правое предсердие резко увеличивается, начинается застой в большом круге кровообращения. В течение 1-го десятилетия болезни у каждого десятого больного появляется синдром Эйзенменгера — быстро прогрессирующий рост легочного сосудистого сопротивления. В его исходе начинается сброс крови справа налево, который приводит к выраженному цианозу, гипоксии органов и, по сути, это предвестник скорого летального исхода.
При больших по площади дефектах, сопоставимых с диаметром аорты, описанный выше цикл перестройки камер сердца и легочных сосудов происходит в течение нескольких лет. Недостаточность кровообращения - причина летального исхода. Меньшие по площади дефекты характерны для тех подростков и взрослых больных, которые попадают под наблюдение врача. Все описанные процессы, приводящие к перестройке камер сердца и легочных сосудов, происходят и у них однако их скорость менее значительна.
По результатам исследования, основанного на данных 25-летнего наблюдения за 1280 пациентами с дефектом межжелудочковой перегородки, установлено, что в группе леченных больных (хирургически и медикаментозно) выживаемость - 87%. Анализ клинического состояния взрослых больных пришедших на прием к врачу, показал, что у3 из них имеют выраженные и умеренно выраженные морфофункциональные изменения камер сердца и легочных артерий. Синдром Эйзенменгера диагностирован у 10% больных.
Диагностика дефекта межжелудочковой перегородки
Жалобы больного зависят от стадии болезни, и в первую очередь определяются степенью легочной гипертензии. В 3-4-м десятилетии болезни легочная гипертензия у неоперированных больных очевидна и приводит к появлению одышки при умеренной физической нагрузке или в покое, утомляемости. Специфические для дефекта межжелудочковой перегородки жалобы отсутсвуют, они идентичны жалобам больных ХСН.
На начальных этапах, до развития синдрома Эйзенменгера, результаты осмотра больного малоинформативны. Можно увидеть систолическое выбухание правого желудочка, которое свидетельствует о его перегрузке объемом крови и давлением. Для терминальной стадии болезни характерно набухание сосудов шеи и диффузный цианоз. Если терминальная стадия болезни наступила в подростковом возрасте, то обнаруживают синдром «барабанных палочек».
Пальпаторно удается определить выбухающий и разлитой верхушечный толчок, смещенный влево и вниз, сочетающийся с сердечным толчком.
Самый ранний диагностический признак болезни - патологиче-скии шум, который появляется при сбросе крови слева направо Его интенсивность меняется с продолжительностью заболевания и отражает морфофункциональную перестройку желудочков сердца и легочной артерии. В начале болезни систолический шум грубый, занимает всю систолу, максимум шума по центру грудины, не проводится в аксилярную зону. По мере протрессирования легочной гипертензии шум ослабевает. Анализ динамики шума — абсолютная компетенция врача. Полное и объективное отражение аускультативной картины в истории болезни, мониторинг интенсивности шума приобретают важное значение для выбора срока хирургического лечения болезни.
Динамика I тона отражает ремоделирование левого желудочка. Степень ослабления I тона пропорциональна степени ослабления систолического шума, обусловленного дефекта межжелудочковой перегородки. На последующих этапах болезни к типичной аускультативной картине присоединится картина трикуспидальной недостаточности и относительного стеноза легочной артерии. Из-за пролабирования створки аортального клапана у 5% больных появляется диастолический шум во 2-й и 5-й точках аускультации сердца. При типичном течении болезни аускультативная диагностика болезни не вызывает затруднений.
Не существует характерных только для дефекта межжелудочковой перегородки электрокардиографических признаков: фиксируют изменения, характерные для гипертрофии ЛЖ и ПЖ. Часто регистрируют АВ-блокаду I степени.
Основа диагностики — эхокардиография Традиционный доступ позволяет верифицировать дефект, его площадь, локализацию и оценить объем сброса крови. Для оценки прогноза и лечебной тактики важна оценка величины правого желудочка, что косвенно свидетельствует о легочной гипертензии.
Катетеризацию полостей сердца выполняют для принятия окончательного решения о целесообразности хирургического лечения больного.
Лечение больного с дефектом межжелудочковой перегородки
Небольшие ДМЖП не требуют какого-либо лечения — достаточно профилактики инфекционного эндокардита. СН, обусловленная ДМЖП в младенчестве, сначала лечится консервативно дигоксином и диуретиками. Постоянная сердечная недостаточность — показание к хирургическому лечению дефекта. Чрескожные устройства для закрытия дефекта уже разработаны.
Допплер-ЭхоКГ позволяет выявить все дефекты небольшого размера, которые склонны к спонтанному закрытию. Синдром Эйзенменгера предупреждают, выявляя признаки повышенного лёгочного сопротивления (серия ЭКГ и ЭхоКГ) и вовремя назначая хирургическое лечение. Хирургическое закрытие дефекта противопоказано при полностью развившемся синдроме Эйзенменгера.
Значительный дефект межжелудочковой перегородки и обусловленный им рост легочного сосудистого сопротивления требуют хирургического лечения в максимально ранние сроки (в раннем детстве). Неоперированные дети умирают до подросткового возраста.
Исходя из этого врач сталкивается:
- с подростком с выраженной легочной гипертензией и синдромом Эйзенменгера, вследствие которых не оперированным в более ранние сроки;
- со взрослым больным, у которого площадь дефекта изначально мала, что позволило ему дожить до среднего возраста без операции;
- с оперированным больным.
Общие принципы ведения больных с дефектом межжелудочковой перегородки.
- Уровень легочного сосудистого сопротивления — главный показатель, определяющий прогноз болезни и исход операции. Если легочное сосудистое сопротивление не превышает уз величины общего сосудистого сопротивления, то операция предотвращает дальнейшую нефункциональную перестройку легочных сосудов
- Хирургическая коррекция дефекта межжелудочковой перегородки, выполненная при легочном сосудистом сопротивлении >1/3 общего сосудистого сопротивления, не останавливает прогрессирование легочной гипертензии.
- Турбулентное движение крови в дефекте МЖП способствует возникновению ИЭ. В связи с этим его профилактика обязательна для больных ДМЖП.
- Все больные с дефектом межжелудочковой перегородки имеют высокий риск внезапной смерти. В постоперационном периоде он достигает 2%. В связи с этим холтер-мониторирование обязательно как в до-, так и послеоперационном периоде. Вопрос о выборе и эффективности антиаритмических препаратов у больных с ДМЖП остается нерешенным.
- В связи с отсутствием исследования оценки эффективности медикаментозного лечения больных с дефектом межжелудочковой перегородки до операции, эту тактику необходимо вырабатывать совместно с хирургом. Можно предположить, что традиционные препараты для лечения ХСН эффективны и для лечения больных с ДМЖП.
- У больных с ДМЖП необходимо достижение целевого АД. Высокое АД приводит к росту сброса слева направо.
- Если у больного с ДМЖП появляется мерцательная аритмия, тактика лечения должна быть направлена на контроль частоты, а не ритма. Контроль состояния свертывающей системы крови у пациентов с дефектом межжелудочковой перегородки и мерцательной аритмией — важная составляющая лечения. MHO необходимо поддерживать на уровне 2-2,5.
- При присоединении ИБС следует обсуждать вопрос об одномоментном вмешательстве на коронарной артерии и коррекции дефекта МЖП.
- В послеоперационном периоде при отсутствии роста легочной гипертензии тактика ведения пациента направлена на предотвращение ремоделирования камер сердца, при росте легочной гипертензии — на ее коррекцию.
Мероприятия по стабилизации состояния больного направлены на то, чтобы выиграть время для окончательного восстановления целостности стенки миокарда. Лечение гипотензии и отека легких производят по описанным повсеместно принципам. Ниже представлены наиболее важные положения:
- Для проведения адекватной гемодинамической поддержки необходим инвазивный мониторинг (катетеризация артерии и легочной артерии). Потребность в инфузионной терапии или диуретиках определяет состояние ПЖ и давление заклинивания легочных капилляров (ДЗЛК). Сердечный выброс, среднее АД и сосудистое сопротивление определяют потребность в вазодилататорах.
- Если систолическое АД >110, с целью уменьшения сосудистого сопротивления и выраженности шунтирования назначают вазодилататоры, обычно начинают с натрия нитропруссида Нитраты расширяют вены, что приводит к усилению шунтирования, в связи с чем их назначения следует избегать. Вазодилататоры не назначают при нарушении функций почек.
- У пациентов с тяжелой гипотензией показано назначение препаратов с инотропными свойствами (вначале добутамина, но в зависимости от гемодинамического эффекта может потребоваться введение эпинефрина). Повышение АД уменьшает выраженность шунтирования.
- В большинстве случаев показана быстрая установка внутриаортапьного баллона для проведения баллонной контрпульсации.
- Как можно раньше следует связаться с хирургом с целью решения вопроса о хирургическом лечении. Операционная летальность продолжает оставаться высокой (20-70%), особенно на фоне интраоперационного шока, задненижнего ОИМ и инфаркта правого желудочка. Сейчас следуют рекомендациям о проведении сопряженного с высоким риском коронарного шунтирования и пластики или протезировании митрального клапана.
- При постепенной отмене лекарственной терапии и механических методов лечения с целью достижения некоторого заживления в области инфаркта проведение хирургического вмешательства может быть отсрочено на 2-4 нед.
- Идеально проведение катетеризации перед операцией с целью выявления сосуда, который будет подвергнут шунтированию.
- Закрытие дефекта перегородки с помощью катетера или напоминающего зонд устройства обеспечивает стабилизацию состояния пациента до тех пор, пока не станет возможным проведение окончательного лечения.
Прогноз при дефекте межжелудочковой перегородки
За исключением синдрома Эйзенменгера, долгосрочный прогноз весьма благоприятней при врождённых ДМЖП. Многие больные с синдромом Эйзенменгера умирают во II или III декаде жизни, незначительная часть пациентов доживает до V декады без трансплантации.
