Гипертрофическая кардиомиопатия: что это такое, лечение, симптомы, признаки, причины
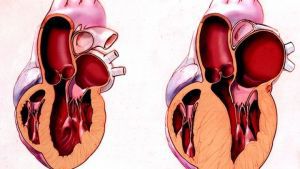
Существует значительное фенотипическое разнообразие, встречают концентрический, верхушечный или полостной варианты гипертрофии (последний часто сопровождают внутриполостной градиент давления и аневризма верхушки сердца).
Кроме того, генетические исследования показали, что у членов семьи пациента, имеющих одинаковые с ним генетические мутации, гипертрофия левого желудочка может практически не развиваться (неполная пенетрантность). Причины такого феномена неясны, но, скорее всего, они мультифакторны.
В некоторых семьях гипертрофическую кардиомиопатию могут сопровождать дополнительные атриовентрикулярные пути проведения и аномальная проводимость.
Что такое гипертрофическая кардиомиопатия
Гипертрофическая кардиомиопатия — заболевание сердца преимущественно наследственной этиологии, при котором развивается неравномерная гипертрофия миокарда. Гипертрофическая кардиомиопатия (ГКМП) — частая форма КМП (распространённость около 100 на 100 000), которая характеризуется непропорциональной и сложной гипертрофией ЛЖ с неправильным расположением мышечных волокон. Гипертрофия может быть генерализованной или преимущественно затрагивать межжелудочковую перегородку и другие области (например, ГКМП верхушки, типичный вариант на Дальнем Востоке).
Причины гипертрофической кардиомиопатии
СН может развиться из-за того, что жёсткие и несинхронно сокращающиеся желудочки препятствуют диастолическому наполнению. Гипертрофия перегородки может также вызвать динамическую обструкцию выводного тракта ЛЖ (гипертрофическая обструктивная кардиомиопатия) или митральную регургитацию. Возникающие при нагрузке симптомы, аритмия и внезапная смерть — главные клинические проблемы.
Данное состояние — генетическое заболевание с аутосомно-доминантным типом передачи, высокой степенью пенетрантности, различной экспрессией. Существуют три типичные группы мутаций с разным фенотипом. Мутации тяжёлых цепей β-миозина ассоциируются с выраженной желудочковой гипертрофией. Мутации тропонина связаны с небольшой, иногда даже с отсутствующей гипертрофией, но выраженной перестройкой волокон миокарда, аномальным сосудистым ответом (например, индуцированная нагрузкой гипотония) и увеличенным риском внезапной смерти. Мутации в миозинсвязывающем белке С имеют тенденцию к позднему развитию и часто ассоциируются с гипертонией и аритмией.
Анализируя приведенное определение, следует остановиться на нескольких пунктах. Во-первых, для гипертрофической кардиомиопатии (ГКМП), в отличие от ДКМП, более четко определена роль наследственных факторов. Доля семейных случаев ГКМП составляет около 50%.
Установлены гены, кодирующие ряд белков саркомера (сократительных белков), мутации которых связаны с возникновением и развитием заболевания. На сегодня описано уже около 400 подобных мутаций в 11 генах.
К этим белкам относятся:
- β-тяжелые цепи миозина (30% белков миокарда, частота мутаций от общего числа мутаций — 30-50 %, на данный момент известно 80 мутаций);
- сердечный тропонин Т (5 % белков миофибрилл, частота мутаций — 10-15%, известных мутаций — более 20);
- α-тропомиозин (5 % белков миофибрилл, частота мутаций — менее 5%, известных мутаций — 8);
- Тропонин I;
- миозинсвязывающий белок С;
- мышечный I.IM-протеин, кодируемый СИРЗ-геном (открыт недавно; является регуляторным белком, осуществляющим дифференцировку кардиомиоцитов, а также взаимодействие белков цитоскелета).
Также в определении говорится о неравномерном характере гипертрофии, т.е. чаще в процесс вовлекаются отдельные сегменты миокарда, хотя возможно и равномерное поражение всего левого желудочка.
Гипертрофическая кардиомиопатия — генетически обусловленное аутосомно-доминантное заболевание. Однако существуют аллельные и неаллельные гетерогенные гены с множественными мутациями. В настоящее время выявлено 10 генов, ответственных за развитие данной патологии. Большинство из этих мутаций происходит в генах, ответственных за кодирование белков саркомеров (например, тяжелых цепей α-миозина, α-тропомиозина, тропонинов).
В отличие от дилатационной кардиомиопатии, такие мутации часто поражают белки саркомеров, участвующих в генерации сердечных сокращений, а не в их передаче. Тем не менее есть случаи, когда в одних и тех же генах наблюдают различные мутации, приводящие как к гипертрофической, так и к дилатационной кардиомиопатии (например, в гене α-актина). Обнаружены также мутации генов, кодирующих белки, не относимые к саркомерным.
Гистологически наблюдают нарушение взаиморасположения миофибрилл и выраженный фиброз. Мелкие внутристеночные артериолы также подвергаются гипертрофии. Изменения могут располагаться в виде чередующихся участков и преобладают в межжелудочковой перегородке. Подклапанная обструкция возникает между передней створкой митрального клапана и гипертрофированной перегородкой. Митральный клапан в систолу двигается в переднем направлении (сочетание разобщенной работы сосочковых мышц и высокой скорости потока в выносящем тракте желудочка). Происходит утолщение клапана и развитие митральной недостаточности.
Патогенез гипертрофической кардиомиопатии
Сейчас существует лишь одна гипотеза развития ГКМП, которая подтверждается большинством экспериментальных и клинических данных. Исходя из этой гипотезы, патогенез ГKMП можно представить следующим образом. В результате различных мутаций белки саркомера теряют способность полноценно функционировать, т.е. снижается их сократительная функция. Механизм здесь заключается в основном в нарушении взаимодействия (3-тяжелых цепей миозина с актином. В результате в кардиомиоцигах начинается избыточный компенсаторный ресинтез этих белков, что и приводит к развитию гипертрофии. Более высокая выраженность процесса в левом желудочке объясняется, по-видимому, большей гемодинамической нагрузкой на него. Однако можно сказать, что гипертрофия в данном случае носит скорее «псевдокомпенсаторный характер», поскольку сократительная способность сердца не только не улучшается, но становится даже хуже. Это связано с тем, что ресинтез сократительных белков осуществляется по программе все тех же дефектных генов, содержащих те или иные мутации. Таким образом, вновь синтезированные белки сократительную функцию выполняют по-прежнему неадекватно.
Кроме того, нарушается диастолическая функция сердца вследствие неполноценного расслабления желудочков в целом, а также асинхронии расслабления отдельных участков миокарда. В определенной степени развитию патологического процесса способствует перегрузка кардиомиоцитов ионами Са2+, приводящая к ухудшению расслабления миокарда во время диастолы.
Определенную роль играет наследственно обусловленное повышение чувствительности адренорецепторов кардиомиоцитов к катехоламинам в период эмбриогенеза. Однако, как показали недавние исследования, два последних механизма не играют первостепенной роли в патогенезе ГКМП. Они лишь способствуют развитию основного процесса, связанного с дефектами сократительных белков.
Морфологические изменения миокарда
Основные отличительные признаки ГКМ1L при микроскопическом исследовании ткани миокарда:
- гипертрофия кардиомиоцитов, толщина которых может увеличиваться в 2 раза и более;
- дезорганизация кардиомиоцитов, заключающаяся в неупорядоченном, хаотичном их расположении, наличии необычных связей между клетками. Данный признак характерен и для других (вторичных) форм кардиомиопатии, но при ГКМП степень выраженности и распространенности намного выше;
- интерстициальный фиброз и очаговый заместительный склероз, обусловленный, по-видимому, очаговым ишемическим повреждением;
- появление интрамиокардиальных артериол с утолщенными стенками.
Симптомы и признаки гипертрофической кардиомиопатии
- Кардиалгия, одышка, перебои в области сердца, сердцебиение, быстрая утомляемость, обморочные состояния.
- Объективные признаки гииертрофии левого желудочка, выявляемые физикальными методами, а также по ЭКГ.
- Нарушения сердечного ритма: экстрасистолии, нарушения внутрижелудочковой проводимости, фибрилляция предсердий.
- Признаки ишемии миокарда.
- Сердечная недостаточность, которая развивается при длительном течении и позже, чем у больных с ДКМП. Таким образом, данный синдром не является для ГКМП ведущим.
Жалобы:
- Стенокардия при нагрузке.
- Одышка при нагрузке.
- Синкопе при нагрузке.
- Внезапная смерть
Физические признаки:
- Высокий скорый пульс.
- Пальпируемый верхушечный толчок (гипертрофия ЛЖ).
- «Двойной импульс» на верхушке (пальпируемый четвёртый тон сердца из-за гипертрофии ЛП).
- Среднесистолический шум на основании сердца.
- Пансистолический шум на верхушке
- Признаки обструкции выходного тракта ЛЖ могут усиливаться в положении пациента стоя (уменьшение венозного возврата), при назначении инотропных средств и вазодилататоров (например, сублингвальных нитратов).
Симптомы и признаки аналогичны аортальному стенозу, за исключением того, что при ГКМП артериальный пульс имеет скачущий характер.
У большинства пациентов ГКМП прогрессирует медленно, в течение нескольких лет. Однако в некоторых случаях возможно стремительное развитие заболевания.
Заболевание часто протекает бессимптомно и выявляется случайно при использовании ЭхоКГ либо при целенаправленном скрининге из-за наличия семейной предрасположенности.
Наиболее часто встречают следующие проявления:
- Возникновение слабости и одышки в связи с нарушением диастолического наполнения и снижения сердечного выброса. Транспорт крови предсердиями очень важен для поддержания сердечного выброса: при ФП симптоматика значительно ухудшается.
- Боль в грудной клетке (приступ стенокардии) может возникать вследствие увеличения работы сердца из-за гипертрофии левого желудочка, дисбаланса потребности и доставки кислорода и снижения кровоснабжения миокарда в результате сдавления интрамуральных артериол. Высокое диастолическое давление приводит к возрастанию диастолического напряжения стенки сердца, что ухудшает кровоток по коронарным артериям в диастолу.
- Предсердные и желудочковые аритмии встречаются нередко и служат причиной предобморочного и обморочного состояний, а также внезапной смерти.
- Предобморочное состояние и обмороки могут возникать при физической нагрузке в результате усиления обструкции выносящего тракта, относительной внутрисосудистой дегидратации или выполнения определенных проб (например, пробы Вальсальвы).
- Приблизительно у 10-15% больных возможно развитие, в конечном счете, дилатации левого желудочка и его недостаточности.
Осложнения ГКМП
- Внезапная смерть.
- Фибрилляция предсердий с отрывом пристеночных тромбов и эмболией.
- Инфекционный эндокардит.
- Хроническая сердечная недостаточность.
Внезапная сердечная смерть
Выявить группу риска при гипертрофической кардиомиопатии чрезвычайно трудно, так как отмечается фенотипическая вариабельность, а большинство факторов риска имеют низкую чувствительность и специфичность.
Естественное течение различно, клиническое ухудшение происходит медленно. Предполагается, что причиной большинства смертей явилась желудочковая аритмия.
Факторы риска внезапной смерти при ГКМП:
- Остановка сердца.
- Повторяющиеся синкопе.
- Неблагоприятный генотип и/или семейный анамнез.
- Индуцируемая нагрузкой гипотония.
- Выраженное увеличение толщины стенки ЛЖ
Маркёры при гипертрофической кардиомиопатии
- Выявление заболевания в молодом возрасте.
- Наличие среди родственников внезапной смерти от недостаточности сердца.
- Кратковременные эпизоды ЖТ при амбулаторном ЭКГ-мониторинге
- Патологический ответ АД на физическую нагрузку.
- Определенные генетические мутации.
Диагностика
Диагноз основан на проведении осмотра, ЭКГ и ЭхоКГ. Необходимо уделять внимание семейному анамнезу и проведению скрининговых исследований среди членов семьи. У некоторых лиц с отягощенным семейным анамнезом по гипертрофической кардиомиопатии можно установить диагноз на основании генетического исследования. Не смотря на выраженную генетическую гетерогенность, диагноз можно подтвердить генетически у 70% пациентов с врожденной гипертрофической кардиомиопатией, что позволяет проводить скрининг других членов семьи больного.
ЭКГ обычно изменена и может содержать признаки гипертрофии ЛЖ с широким рядом странных изменений (например, псевдоинфарктная картина, глубокая инверсия зубца 7). ЭхоКГ обычно помогает установить диагноз, однако это бывает сложно при наличии других причин гипертрофии ЛЖ (например, физические нагрузки — спортивное сердце, АГ), но выраженность гипертрофии обычно выше ожидаемой. Генетическое исследование поможет в будущем поставить диагноз.
Осмотр
Обструкция выносящего тракта может проявляться двойным верхушечным толчком и систолическим шумом, начинающимся в середине систолы. Шум усиливается при выполнении больным пробы Вальсальвы или приседаний. Может наблюдаться пансистолический шум митральной недостаточности вследствие движения вперед створок митрального клапана в систолу.
Методы исследования
ЭКГ редко остается неизмененной. Характерны вольтажные признаки гипертрофии с нарушением реполяризации:
- Гипертрофия с изменениями сегмента ST и зубца Т.
- Глубокий зубец О в нижних и боковых отведениях, свидетельствующий о гипертрофии межжелудочковой перегородки.
- Преждевременное возбуждение и синдром Вольфа-Паркинсона-Уайта.
- Желудочковые экстрасистолы.
ЭхоКГ — обязательный метод, позволяющий с высокой точностью установить размер камер сердца и толщину стенок. С его помощью также облегчается визуализация выносящего тракта или внутриполостных градиентов:
- Асимметричная гипертрофия перегородки — значительное утолщение перегородки, уменьшение ее подвижности.
- Уменьшение полости у левого желудочка с гиперкинезом задней стенки.
- Закрытие створок аортального клапана в середину систолы или своеобразное трепетание их концов.
- Движение митрального клапана вперед во время систолы.
МРТ сердца полезно в сомнительных случаях.
Другие методы исследования могут помочь в стратификации риска, хотя ни один из них неспособен оценить риск возникновения внезапной сердечной смерти. Отрицательные результаты исследований также не исключают риск развития синдрома внезапной смерти:
- Амбулаторный мониторинг ЭКГ. Позволяет обнаружить предсердные и желудочковые аритмии.
- Пробы с физической нагрузкой. Позволяют оценить функциональный резерв сердца и ответ АД на физическую нагрузку.
- Катетеризация сердца. Позволяет визуализировать анатомию сердца и его полостей, градиент давления выносящего тракта и внутри полости левого желудочка.
- Электрофизиологическое исследование. Использование вызванных потенциалов позволяет выявить дополнительные пути проведения.
- Генетическое исследование. Имеет ценность для скрининга членов семьи после выявления дефектного гена у пробанда.
Лечение гипертрофической кардиомиопатии
- Ограничение физической нагрузки.
- Лекарственная терапия:
- β-блокаторы (пропранолол);
- антагонисты Са2+ (верапамил);
- антиаритмические средства (амиодарон) — при наличии желудочковых нарушений ритма.
- Хирургическое лечение:
- при наличии риска внезапной сердечной смерти показана имплантация кардиовертера-дефибриллятора;
- при отсутствии эффекта от консервативной терапии и ухудшении показателей внутрисердечной гемодинамики прибегают к хирургическому лечению.
- Дополнительные методы лечения.
Большие надежды возлагаются на генную терапию. Период полужизни миозина составляет примерно 5 дней. Другие белки миокарда живут еще меньше. Поэтому белковый состав сердца полностью обновляется в течение нескольких недель. В случае удачного ингибирования мутантной аллели можно, по-видимому, будет добиться восстановления структуры сократительных белков и, как следствие, регрессии гипертрофии.
β-Адреноблокаторы и снижающие ЧСС антагонисты кальция (например, верапамил) могут облегчать приступы стенокардии и иногда предупреждать приступы синкопе; однако не существует консервативного лечения, которое бы определённо улучшало прогноз. Аритмии встречаются часто и обычно отвечают на лечение амиодароном. Обструкцию выходного тракта можно уменьшить с помощью частичной хирургической резекции (миоэктомия) или ятрогенного инфаркта базальной перегородки (септальная аблация) с помощью транскатетерного введения спиртового раствора. Имплантируемый кардиовертер-дефибриллятор показан больным с риском развития внезапной смерти. Дигоксин и вазодилататоры увеличивают обструкцию выводного тракта и противопоказаны.
Приблизительно половина всех случаев внезапной смерти от гипертрофической кардиомиопатии происходит во время или сразу после тяжелых физических нагрузок. Поэтому всем пациентам с данной патологией необходимо избегать соревновательных видов спорта. К сожалению, значительная часть пациентов умирают внезапно без каких-либо предвестников. Медикаментозное лечение обычно включает назначение следующих групп препаратов.
β-Адреноблокаторы. Препараты снижают потребность миокарда в кислороде и улучшают диастолическое наполнение левого желудочка, уменьшают одышку и выраженность боли в груди. Основные средства для лечения приступов стенокардии, одышки, головокружения и обмороков. Может потребоваться назначение больших доз.
Дизопирамид. Обладает отрицательным инотропным и антиаритмическим действием, уменьшает градиент давления выносящего тракта. К сожалению, его применение ограничено ввиду наличия у него побочных эффектов, связанных с антихолинергическими свойствами.
Антиаритмики. Использование антиаритмических препаратов, таких как амиодарон и сотапол, позволяет устранить наджелудочковые аритмии, но не снижает риск смерти от фатальной ЖТ. При возникновении ФП необходимо скорейшее выполнение кардиоверсии (использование амиодарона увеличивает шансы на успех). При неудаче кардиоверсии возможно назначение дигоксина.
Нефармакологические методы лечения
- Двухкамерная стимуляция сердца с короткой атриовентрикулярной задержкой применяется у пациентов с признаками обструкции и рефрактерностью к медикаментозной терапии. Вызывая предвозбуждение желудочка, добиваются десинхронизации сокращений левого желудочка, что уменьшает градиент в выносящем тракте левого желудочка. Достижение устойчивой многократной деполяризации правого желудочка достаточно сложно, особенно при физической нагрузке, а слишком большая атриовентрикулярная задержка может нарушать диастолическое наполнение.
- Абляция межжелудочковой перегородки спиртом достигается выполнением инъекций спирта в первую или вторую перфорирующие артерии межжелудочковой перегородки. Эта процедура вызывает развитие локализованного ИМ гипертрофированной проксимальной части межжелудочковой перегородки, что уменьшает градиент давления выносящего тракта левого желудочка. Однако значительное количество больных (10-15%) после выполнения данной манипуляции нуждается в проведении постоянной электрокардиостимуляции из-за развития атриовентрикулярной блокады. Теоретически увеличивается риск развития желудочковых аритмий, так как создается благоприятный субстрат для последующего их развития.
- Хирургические методы: выполнение миотомии-миоэктомии проксимальной части межжелудочковой перегородки (операция Морроу). В отдаленном периоде возможно развитие осложнений, включая аортальную недостаточность. При развитии у пациентов дилатации левого желудочка и систолической сердечной недостаточности может потребоваться пересадке сердца.
- Необходимо рассмотреть целесообразность установки кардиовертера-дефибриллятора пациентам, перенесшим остановку сердца или имеющим ЖТ с нестабильной гемодинамикой.
