Система гемостаза (процесс образования клеток крови): методы исследования, диагностика, схема, факторы, показатели, норма, нарушение
В процессе эволюции сформированы весьма эффективные механизмы, направленные на поддержание функции кровообращения как транспортной системы.
К ним относят те, которые предотвращают потерю крови в случае повреждения сосуда, обеспечивая гемостаз, а также не позволяют кровотоку прерваться из-за тромбоза. Выделяют две фазы гемостаза: клеточную (сосудисто-тромбоцитарную) и гуморальную (коагуляционную). В начале клеточной фазы сосуд в месте повреждения сокращается, и здесь же происходит агрегация тромбоцитов и формирование тромбоцитарной пробки, призванной остановить кровотечение. Это занимает несколько минут. Далее активируется система свёртывания, в результате которой образуется фибриновая сеть, упрочняющая тромбоцитарную пробку. Эти две фазы тесно связаны между собой. Повреждённые эндотелий и субэндотелиальный матрикс активируют тромбоциты; те, в свою очередь, создают идеальные условия для фиксации плазменных факторов свёртывания с образованием нерастворимого фибрина.
В организме кровь перемещается по кровеносным сосудам, состоит из плазмы и клеточных элементов трёх видов:
- эритроцитов;
- лейкоцитов;
- тромбоцитов, обеспечивающих взаимодействия между стенками кровеносных сосудов и факторами свёртывания, что, в конечном итоге, поддерживает целостность сосудистой системы.
Органы гемопоэза
К V месяцу внутриутробного развития плацдармом для гемопоэза становится костный мозг. При рождении гемопоэтический костный мозг находится в медуллярных пространствах всех костей, но с возрастом он постепенно замещается жиром (жёлтый костный мозг). По достижении организмом зрелости гемопоэз происходит практически только в позвонках, тазовых костях, грудине, рёбрах, ключицах, черепе, в проксимальных отделах плечевых и бедренных костей.
Костный мозг занимает межтрабекулярные пространства кости и содержит весь спектр гемопоэтических клеток-предшественников и определённый пул зрелых клеток, предназначенный для выхода в кровь в случае необходимости. Гемопоэтические клетки соседствуют и тесно взаимодействуют с соединительнотканной стромой, в том числе с ретикулярными клетками, макрофагами, жировыми клетками. Строма на микроуровне обеспечивает надлежащие условия для роста и развития клеток крови. Для здорового костного мозга характерна особая организация. Расположенные гнёздами клетки-предшественницы эритроидного ряда окружают центральный макрофаг, который обеспечивает их железом и фагоцитирует вытесняемые из клеток ядра. Мегакариоциты — крупные клетки. От них отшнуровываются тромбоциты, которые затем направляются в сосудистые синусы. Клетки-предшественницы лейкоцитов группируются поблизости от костных трабекул. Созревающие клетки мигрируют по свободным пространствам костного мозга по направлению к сосудистым синусам. Доля плазматических клеток, как правило, не превышает 5%. Все они распределены по межтрабекулярным пространствам.
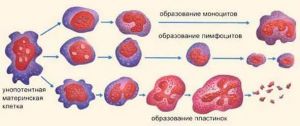
Образование клеток крови
Стволовые клетки
Гемопоэз — активный процесс, который призван поддерживать количество циркулирующих клеток крови в нормальных пределах и быстро отвечать на повышенные требования к нему, например, при кровотечении или инфекции. Факторы роста часто взаимодействуют между собой на принципах синергизма. Многие из этих факторов роста теперь синтезируют с помощью технологии рекомбинантной ДНК и их используют в качестве лекарств.
Последние открытия учёных предполагают, что в костном мозге есть стволовые клетки, которые, помимо клеток крови, способны дифференцироваться до клеток других тканей, в том числе нервной, костной, мышечной, миокардиальной, печёночной и эндотелия кровеносных сосудов. Это свойство называют пластичностью стволовых клеток, и в будущем оно может открыть потрясающие возможности клинического применения.
Эритроциты
Клетки-предшественницы эритроцитов, развившиеся из недифференцированной родоначальной клетки, называют эритробластами или нормобластами. Эти ядросодержащие клетки делятся и постепенно накапливают в себе гемоглобин, который придаёт цитоплазме розовую окраску. Ядро клетки затем конденсируется и элеминируется из неё. Первая безъядерная красная клетка называется ретикулоцитом. В её цитоплазме пока ещё остаётся рибосомный материал. При обычной окраске ретикулоциты выглядят как большие эритроциты с лёгким голубым оттенком, именуемым полихромазией. Ретикулоциты утрачивают рибосомы и созревают в течение 3 сут, в течение которых переходят в кровоток. Увеличение количества циркулирующих в крови ретикулоцитов (ретикулоцитоз) говорит об усилении эритропоэза. Процесс созревания эритроцитов контролируют эритропоэтин, полипептидный гормон, который синтезируют клетки, образующие выстилку почечных канальцев, в ответ на гипоксию. У лиц, страдающих почечной недостаточностью, развивается анемия из-за недостаточной продукции эритропоэтина. Для лечения этого состояния применяют экзогенный рекомбинантный гормон.
Лейкоциты
В костном мозге существует большой запас зрелых нейтрофилов. Ежедневно в кровоток выходит около 1014 нейтрофилов. Клетки свободно циркулируют или прикрепляются к эндотелию и формируют маргинальный пул. Эти два пула клеток равны. Нейтрофилы остаются в циркуляции 6—10 ч, после чего удаляются из крови, главным образом, селезёнкой. В другом случае они переходят в ткани и расходуются на протекание воспалительного процесса или подвергаются апоптозу, и их фагоцитируют макрофаги. Миелоциты и метамиелоциты обычно обнаруживают только в костном мозге, но при инфекциях или интоксикациях они могут появиться в периферической крови. Обнаружение молодых форм миелоидного ростка в крови часто сочетается с присутствием ядросодержащих эритроцитов. Такое состояние называют лейкоэритробластной трансформацией, которая указывает на резко выраженное нарушение функции костного мозга. Моноциты — крупные клетки превращаются в макрофаги. Последние способны пролиферировать годами. Такие цитокины, как Г-КСФ, ГМ-КСФ и М-КСФ, участвуют в созревании клеток миелоидного ряда, поэтому их можно использовать для лечения больных, например для того, чтобы ускорить восстановление числа нейтрофилов в крови после химиотерапии.
Тромбоциты
Тромбоциты происходят из мегакариоцитов. Мегакариоцитарные стволовые клетки (КОЕ-Мег) делятся и образуют мегакариобласты. При созревании мегакариоцитов происходит эндомитотическая редупликация, в процессе которой делится ядро, но не сама клетка. В итоге зрелые мегакариоциты представляют собой крупные клетки с несколькими ядрами и цитоплазмой, содержащей тромбоцитарные гранулы. От каждого мегакариоцита на уровне синусов костного мозга отшнуровывается и поступает в кровоток до 3000 тромбоцитов. На формирование и созревание мегакариоцитов влияет тромбопоэтин. Рекомбинантную форму этого цитокина применяют в клинической практике. До разрушения в органах ретикулоэндотелиальной системы тромбоциты циркулируют на протяжении 8—14 сут. Приблизительно 30% тромбоцитов периферической крови обычно секвестрировано в селезёнке.
Фибринолиз
У здоровых людей патологическое образование фибрина в кровяном русле предотвращается фибринолитической системой. Главный пусковой фактор, запускающий работу этой системы, — тканевый активатор плазминогена (tPA), который высвобождается из эндотелиальных клеток. В какой-то мере фибринолиз стимулируется также активатором урокиназы, которую синтезируют почки, чтобы защитить себя от обструкции мочевыводящих путей микросгустками крови. Эти активаторы превращают циркулирующий неактивный зимоген-плазминоген в активный фермент плазмин, который растворяет фибрин. Внутри сосудистого тромба оба tPA и плазминоген связываются с нерастворимым фибрином, образуется плазмин, который лизирует тромб. Фрагменты находящегося в процессе расщепления фибрина и D-димеры можно обнаружить в кровотоке. При наличии венозного тромбоза их концентрация повышается.
Чрезмерно высокая концентрация tPA в крови блокируется присутствием ещё одного вещества в плазме, ИАП; плазмин инактивируется α2-антиплазмином.
Обследование
Клинический анализ крови
Кровь, обработанную антикоагулянтом, пропускают через автоматический анализатор, который на основе специальных технологий (распределение клеток по размеру, радиочастотный анализ, методы с использованием лазерного луча) выдаёт заданный спектр гематологических параметров. Среди них количество клеточных элементов, доля эритроцитов в крови (гематокрит, Ht), эритроцитарные индексы, информирующие об их размере (средний корпускулярный объём, MCV) и количестве гемоглобина в эритроцитах (среднее насыщение клетки гемоглобином, МСН). Современные анализаторы способны дифференцировать клетки крови и предоставить лейкоцитарную формулу с указанием количества нейтрофилов, лимфоцитов, моноцитов, эозинофилов и базофилов. Однако важно понимать, что ряд условий может привести к ложным результатам.
Ложные результаты клинического анализа крови при использовании анализатора
| Результат | Объяснение |
|---|---|
| Завышение уровня гемоглобина | Гиперлипидемия, желтуха, очень высокий лейкоцитоз |
| Занижение уровня гемоглобина | Неправильное смешивание образца крови с реактивом; взятие крови из вены, через которую осуществлялась инфузия растворов |
| Завышение объёма эритроцитов (MCV) | Присутствие холодовых агглютининов; гиперосмолярность, не связанная с кетонемией |
| Завышение числа лейкоцитов | Наличие ядросодержащих эритроцитов |
| Занижение числа тромбоцитов | Образование сгустка крови, агрегация тромбоцитов |
Микроскопия мазка крови
Хотя из-за технического прогресса и автоматизации лабораторных исследований потребность в микроскопии мазков крови почти отпала, отнюдь не редко тщательное изучение их предоставляет бесценную информацию для диагностики. Анализаторы не в состоянии идентифицировать изменения в эритроцитах, их морфологии (тельца Хауэлла—Жолли, базофильные включения, малярийные плазмодии и др.) или дать описание патологических клеток белой крови, например бластов.
Исследование костного мозга
Пунктат костного мозга у взрослых пациентов часто берут из задней части гребня подвздошной кости. Аспирацию проводят под местной анестезией; мазки окрашивают и изучают под микроскопом. Кроме этого метода есть возможность получить столбик губчатой кости (трепанобиопсия). Полученный материал фиксируют, декальцифицируют и делают гистологические срезы с окраской. Микроскопия мазка костного мозга позволяет оценить состав и морфологию гемопоэтических клеток или характеризовать инфильтрацию патологическими клетками. Для дальнейшего углубления диагностики существует возможность анализировать поверхностные клеточные маркёры (иммунофенотипирование), хромосомные и молекулярные особенности клеток, оценить степень злокачественности заболевания или сделать посев костного мозга при подозрении на туберкулёз. Трепанобиопсия — более надёжный метод для определения клеточного состава костного мозга, выявления фиброза и инфильтрации патологическими клетками, например при метастазах рака.
